Химический элемент золото (Au): свойства, способы получения и место в периодической таблице Менделеева
Здравствуйте, золото — это химический элемент, который стоил многих жизней. Когда Исаакиевский собор в Санкт-Петербурге был построен, его купола были сделаны из золота. золотились с помощью золотой Амальгамы. Архитектор Огюст Монферран принял меры по защите рабочих от паров ртути, но обнаружил, что они были обречены на провал. Но купола не должны были этого делать. золотить больше никогда.
Так и случилось: все 60 человек умерли от отравления, а собор с тех пор больше никогда не видели. не золотили.
Нахождение в природе
Золото есть везде. Один кубический километр морской воды содержит 5 килограммов вожделенного элемента, а если уколоть палец и выдавить каплю крови, то в ней будет 0,00025 г. мг золота. В человеческом скелете содержится 10 мг: если вы хотите почувствовать запах кольца людей, вам понадобится всего 300 человек. Но это золото он так широко рассеян в окружающей среде форме, что добывать оттуда нерентабельно, а зачастую и невозможно.
11. Названия химических элементов
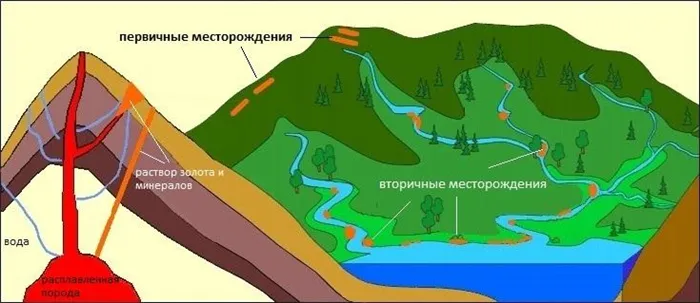
Месторождения, пригодные для добычи полезных ископаемых золота, делятся на метамагматические и россыпные месторождения.
Первичные месторождения
Химическим элементом Au богата магма — плавильный элемент внутри планеты. Золото содержится в верхних слоях мантии Земли и частично в земной коре (которая, однако, содержит почти всю периодическую таблицу). Магма поднимается на поверхность планеты, остывает и превращается в твердую породу. Места, где содержится достаточное количество этого ценного элемента, чтобы промышленная добыча была целесообразной, являются первичными месторождениями.

Природное золото Он находится в виде наггетсов — цельных зерен химически чистого вещества. Он часто сочетается с другими элементами (магма содержит почти все элементы):
- серебром;
- медью;
- металлами платиновой группы;
- висмутом и другими.
Вторичные месторождения
Вторичные отложения являются результатом разрушения первичных отложений, называемого выветриванием:
- физическим (причина — ветер, вода, температурные колебания);
- химическим (химические реакции);
- биологическим (бактерии и другие организмы).
Россыпь чистого золота Они похожи на песок и иногда переносятся водой на многие километры от первоначального месторождения.
История открытия элемента
В чистом виде золото Он попал в руки человека в шестом веке до нашей эры. Массовая добыча африканских месторождений началась раньше, около 2000 года до н.э., но тогда еще не существовало методов удаления примесей, и золотые Продукция этого периода была низкого качества.
В конце античности (начало нашей эры) алхимия начала распространяться по всему миру с ее стремлением превратить низшие химические вещества в благородные. Она не была успешной, но современная цивилизация обязана ей многими чудесами, такими как техника получения химически чистых золота из руды.
Латинское название золота — Aurum (читается как аурум) — «желтый». Она признана международной. Для алхимиков символ солнца выглядел как круг с точкой внутри, но в современной химии он обозначается аббревиатурой Au.
См. также 2006 год, где количество составило 386,6 тонн (без учета свопов). золота (за исключением операций с иностранной валютой). Поделиться золота в общем объёме золотовавалютных резервов в России составляла 3,8% в марте 2006 года. Россия занимает 14-е место в мире по количеству ау золота, мировых запасов.
Химическая справка
Золото обозначается в химии как Aurum, сокращенно Au, в электронном виде: KLMNO6s1, Eион(Ме=>Me++e)=9,22 эВ. В таблице Менделеева золото он имеет атомный номер 79. Он находится в группе 11 шестого часа. Также у золота имеет международный номер CAS: 7440-57-5. Атомный вес элемента составляет 196,9665 г/моль.
Золото — это простое вещество, как оно состоит изотопы металла.
Свойства золота Его свойства уникальны и позволяют использовать его в электронике, медицине и при производстве оборудования для химических лабораторий. Он обладает высокой тепло- и электропроводностью. Именно поэтому тонкопленочное гальваническое покрытие золота Гальваническое покрытие все еще может использоваться в электротехнике. Золото не кипит до 2880 градусов Цельсия, имеет плотность 19,32 г/см3 и температуру плавления 1064,43 °C. Золото достаточно инертно даже при высоких температурах и не вступает в реакцию с другими химическими веществами.
История золота
Название золото назван в честь своего желтого цвета. Его название звучит по-разному на многих языках, но оно имеет отношение к его желтому цвету, золотистили зеленоватого цвета. Золото обладает несколькими важными характеристиками. Это драгоценный металл, потому что он не ржавеет и не вступает в реакцию окисления при воздействии элементов окружающей среды.
Кстати, именно по этой причине он успешно используется в стоматологии. Золото имеет высокую плотность, что является основой для его извлечения путем промывки грязи, песка и речной воды. Так и есть, золото он очень мягкий и податливый. Несмотря на свойства металла, его можно поцарапать даже без использования специальных инструментов.

Золото, вероятно, было первым металлом, открытым человеком. Он упоминается во всех сохранившихся источниках древности; он был престижным и довольно дорогим. Несомненно, интерес к золоту никогда не ослабевал. Он ценился за свою красоту и особые свойства, и только позже была признана ценность его физических свойств. Еще до появления химического формула вещества, покупка золота это считалось отличной инвестицией.
Природное золото
В природе золото Его можно найти в виде окаменевших самородков или в виде плит. Если это не зерна, рассеянные в руде или вымытые водой, то это самородки, которые можно разделить на несколько подтипов: Электрум, палладий золото, Cu, висмут. В этом случае химический состав выглядит следующим образом золота также содержит примеси, которые могут варьироваться в процентном соотношении.

Электрум — это сплав с серебром, известный с древних времен. Фактически, это был первый сплав, с которым человеку пришлось иметь дело. Это минерал, который примерно наполовину состоит из частиц серебра. Его название происходит от слова «янтарь», что связано с внешним видом минерала. Сплавы палладия — это соединения с серебром, медью, хромом, никелем и другими веществами.
Висмут золото содержит до 4 % этого серебристо-розового металла. Медь золото содержит до 20% меди, которая придает ему красноватый оттенок. Также возможно образование минералов золота с железом, ртутью, иридием. Аллювиальные золото называется шлиховым, и состоит Вследствие выпадения в осадок тяжелых металлов, к которым и золотые крупицы.
Приоритеты использования драгоценных металлов в стоматологии изменились. До середины двадцатого века считалось престижным иметь золотые зубы (коронки). Однако сегодня драгоценный металл заменяется металлокерамикой и другими более современными материалами. Но люди, которые хотят выглядеть молодо, прошивают зубы. золотые нити под кожу.
Золото

Золото, вероятно, первый металл, с которым человечество вступило в контакт (см. подробнее первый металл России золотодоОдним из первых золотодобытчиков является Ерофей Марков, памятник которому в Екатеринбурге заслуживает внимания.
Об истории добычи золота см. Происхождение названия
Поскольку золото был известен, вероятно, еще до появления письменности, проследить историю его имени невозможно. Известно, однако, что в славянских языках слово золото в древности имело общий корень со словом «желтый»; первоначальный вариант слова пишется как zolto. Некоторые люди связывают происхождение слова «.золото» со словом «солнце» (корень sol). Однако достаточно достоверных версий о происхождении названия нет.
Слово gold в европейских языках связано с греческим богом Солнца Физические свойства
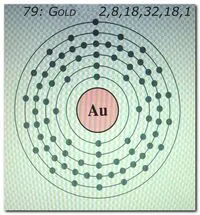
Схема атома золота
Химический элемент в периодической таблице Менделеева, № 79, под номером В. 196.967- относится к драгоценным металлам. Известен только один стабильный изотоп Au197. Из искусственных радиоактивных изотопов наиболее важными являются Au195 и Au198. Конфигурация внешних электронов атома золота. : 5d10 6s1. Энергия ионизации Au+ составляет 9,22 эВ.
Чистое золото — представляет собой мягкий металл чистого желтого цвета. Некоторые продукты приобретают красноватый оттенок. из золота, Красноватый оттенок некоторых изделий, например, монет, может быть обусловлен наличием примесей других металлов, особенно меди. В тонких пленках золото Золото — это полупрозрачный зеленый цвет. Золото обладает чрезвычайно высокой теплопроводностью и низким удельным сопротивлением.
Золото — очень тяжёлый металл: Химические свойства
Золото относительно легко реагирует с кислородом и другими окислителями, содержащими комплексообразователи. В водных растворах цианида, например, при наличии кислорода золото он растворяется и образует цианоаураты:
В реакции с хлором возможность комплексообразования также значительно облегчает процесс реакции: когда с сухим хлором золото реагирует при ~200 °С с образованием Физиологическое воздействие
Содержание золота в земной коре очень мало — 3 мг/т, но месторождений и регионов, сильно обогащенных этим металлом, очень много.
Для золота Шаратерное серебро, которое имеет зеленоватый оттенок и относительно легко разрушается при транспортировке водой. В скалах. золото обычно рассеяно на атомарном уровне. В месторождения оно зачастую заключено в сульфиды и Получение
Промывка
Метод промывки основан на высокой плотности золота, Поэтому минералы с меньшей плотностью в водном потоке являются золота (которые представляют собой почти все минералы земной коры) вымываются, и металл концентрируется в тяжелой фракции — песке. состоящего из минералов повышенной плотности, который называется Амальгамация
Метод амальгамации основан на способности ртути образовывать сплавы — Испании начиная с XVI века: это стало возможным благодаря наличию в Испании огромного ртутного месторождения — Цианирование
Золото растворимо в растворах синильной кислоты и ее солей, и это свойство привело к появлению различных методов добычи путем цианирования руд.
Метод цианирования основан на реакции золота с цианидами в присутствии атмосферного кислорода: щебень. золотоноИзвлеченная порода обрабатывается разбавленным (0,3-0,03%) раствором цианида натрия, золото из полученного раствора цианида натрия NaAu(CN)2 осаждается либо с помощью цинкового порошка, либо с помощью специальных ионообменных смол.
Золотые сплавы в стоматологии
Благодаря высокой коррозионной стойкости и простоте обработки, золото он давно используется в качестве материала для зубных пломб. Для придания изделию высокой прочности используются специальные сплавы.
Традиционно чистота золота измеряется в британских Российская система проб
Система, используемая в России, отличается от мировой. В России чистота золота измеряется См. также
Источник: uhistory.ru
Химический элемент золото (Au): свойства, способы получения и место в периодической таблице Менделеева
Золото — химический элемент, унесший много жизней. При строительстве Исаакиевского собора в Петербурге купола золотились с помощью золотой амальгамы. Архитектор Огюст Монферран принял меры, чтобы защитить рабочих от паров ртути, но понимал, что они обречены. Зато купола не придется золотить больше никогда.
Так и случилось: все 60 человек погибли от отравления, а собор с тех пор ни разу не золотили.
Нахождение в природе
Золото везде. Кубический километр морской воды содержит 5 кг вожделенного элемента, а если уколоть палец и выдавить каплю крови, в ней будет 0,00025 мг золота. 10 мг содержится в человеческом скелете: если задаться целью выплавить кольцо из людей, понадобится всего 300 человек. Но это золото находится в окружающей среде в настолько рассеянной форме, что извлекать его оттуда невыгодно, а часто и невозможно.
Месторождения, подходящие для добычи золота, подразделяются на коренные — первичные (постмагматические) и вторичные (россыпные).
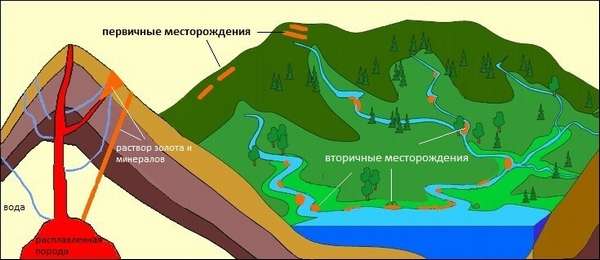
Первичные месторождения
Химическим элементом Au богата магма — расплав внутри земного шара. Золото есть в верхних слоях мантии и частично в земной коре (впрочем, в ней содержится почти вся периодическая таблица). Магма выходит на поверхность планеты, остывает и превращается в твердую породу. Места, где она содержит столько драгоценного элемента, чтобы окупилась промышленная разработка, и есть коренные месторождения.

Природное золото находят в виде самородков — цельных зерен химически чистого вещества. Часто оно соединено с другими элементами (магма содержит почти все):
- серебром,
- медью,
- металлами платиновой группы,
- висмутом и другими.
Вторичные месторождения
Вторичные месторождения — итог разрушения первичных, так называемого выветривания, которое бывает:
- физическим (причина — ветер, вода, температурные колебания),
- химическим (химические реакции),
- биологическим (бактерии и другие организмы).
Россыпь чистого золота выглядит как песок и порой относится водами на много километров от коренного месторождения.
История открытия элемента
В чистом виде золото попало в руки человека в VI веке до нашей эры. Массовые разработки африканских месторождений начались раньше — около 2000 года до н. э., но методик избавления от примесей не было, и золотые изделия того времени имеют низкую пробу.
К прочтению: Характеристика и стоимость серебра 925 пробы в России
Во времена поздней античности (начало нашей эры) по миру начала распространяться алхимия с ее стремлением превращать недрагоценные химические элементы в благородные. Она не добилась успеха, но современная цивилизация благодаря ей владеет многими чудесами — например, техникой добычи химическичистого золота из руды.
Латинское название золота — Aurum (читается как аурум) — «желтый». Оно принято как интернациональное. Символ солнца у алхимиков выглядел как круг с точкой внутри, а в современной химии оно обозначается сокращением Au.
Как получают
Основные способы получения золота в промышленных масштабах дополняют друг друга — например, шлих можно очистить от плотных примесей путем амальгамации.
Промывка
Промывка (шлихование) — древний метод добычи золотого песка (шлиха) из вторичных месторождений. Песок отмывается благодаря плотности: менее плотные минералы вымываются водой, а шлих оседает.
Масштабная добыча золота автоматизирована: вместо людей работают промывочные устройства и экскаваторы. Однако принцип их действия за последние 2000 лет почти не изменился.
Шлих — не чистое золото. Существуют элементы плотнее — они оседают с песком на дне промывочной емкости. Для финальной очистки используются другие, в частности химические, способы.
Амальгамация
Этот метод тоже известен с древности, но описан в XVI веке. Он возможен благодаря свойству ртути образовывать сплавы (амальгамы) с другими металлами без дополнительного термического или химического воздействия. После избавления от фрагментов пустой породы химические элементы механически разделяются.
Всеволод Козловский6 лет в ювелирном деле. Знает все о пробах и может определить подделку за 12 секундАмальгамация применяется не везде: в ряде стран (с 1988 года — в России) запрещено использовать ртуть из-за смертельной опасности этого элемента для человека.
Цианирование
Способ извлечения драгоценного элемента из руды цианированием основывается на способности золота растворяться в синильной кислоте (цианистом водороде, HCN) и ее солях. Руда обрабатывается слабым (0,03–0,3 %) раствором цианида. Благородный металл реагирует раньше других химических элементов, а после химической реакции осаждается из раствора.
Физические и химические свойства
Золото инертно: в чистом виде не образует оксидов, не подвержено коррозии. Еще у него:
- высокая плотность — 19,32 г/см³,
- среднеплавкость (температура плавления в диапазоне 600–1600 °С — 1064,43 °С),
- низкая твёрдость — 2,5 пунктов по шкале Мооса,
- высокая ковкость (благодаря ей создается позолота),
- высокая пластичность, тягучесть.
К прочтению: Самородное золото: характеристика и особенности металла
Место золота в периодической таблице Менделеева
Элемент располагается в XI группе (подгруппа меди), VI периоде периодической таблицы химических элементов.
Атомный номер (зарядовое число) золота — 79. Это количество протонов в ядре атома, равное количеству электронов, вращающихся вокруг ядра. Атомная масса — суммарная масса протонов и нейтронов (ядра атома) — у золота равна 196,9665 а.е.м. (атомных единиц массы). Природное золото существует в виде химически устойчивого изотопа 197 Au. Все остальные нестабильны и возможны только в условиях ядерного реактора.

Формула
Своей химической формулы золото не имеет, поскольку существует в виде одноатомных молекул. Электронная конфигурация атома Au записывается как [Xe] 4f14 5d10 6s1 и обозначает точное распределение электронов по орбиталям.
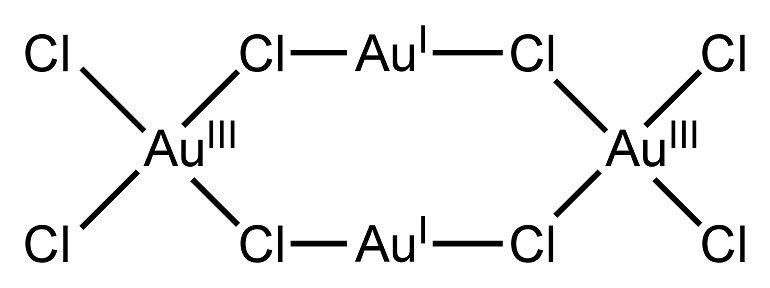
Взаимодействие с кислотами
В силу своей инертности (не абсолютной, но значительной) золото не растворяется в кислотах. Это позволяет использовать их для аффинажа (химической очистки элемента от примесей): сплав обрабатывается кислотой, например азотной, и так избавляется от лигатуры.
Но есть исключения. Чистое золото растворяют кислоты:
- селеновая,
- синильная и ее соли (цианиды),
- азотная в смеси с соляной (царская водка).
Степени окисления и связь с галогенами
В естественных условиях Au не окисляется под воздействием кислорода — это одно из свойств, делающих элемент драгоценным. При нагревании золото взаимодействует с галогенами (элементами XVII группы): йодом, фтором, бромом и хлором, образуя соответственно йодид, фторид, бромид и хлорид.
Стандартные степени окисления — 1 и 3. В лабораторных условиях выведен фторид со степенью окисления +5.
Меры чистоты золота
Государства контролируют оборот драгметалла. Век назад почти в каждой стране работала своя система пробирования, но сейчас большинство приведено к общему знаменателю.
Британская каратная система
В каратной системе (США, Канада, Швейцария) за 100 % принято число 24. Клеймо «18 K» говорит о том, что украшение состоит на 75 % из драгоценного металла, а на 25 % из чего-то ещё — например меди и палладия.

Метрическая система
В России, СНГ, Германии число на клейме — это количество промилле (тысячных долей) золота в сплаве. 500 ‰ — проба 500, 375 ‰ —375. Не существует только пробы 1000 — вместо нее 999,9. Она содержит микроскопическое количество примесей и условно считается чистой.
К прочтению: ТОП-16 эффективных способов, как почистить серебро в домашних условиях + чем нельзя обрабатывать украшения
Золотниковая система
Золотниковая система проб действовала в Российской империи, РСФСР и СССР в 1798–1927 годах. Она основана на русском фунте, равном 96 золотникам, аналогична каратной математически, но делит целое не на 24, а на 96 долей.
Таблица соответствия проб
Посмотрим на три системы в сравнении. Существует также лотовая проба — она по сути повторяет каратную, но берет за сто процентов 16 единиц (лот). Лотовая проба использовалась для пробирования серебра в Европе до введения метрической системы и не имеет отношения к золоту.
| Метрическая система проб | 999 | 958 | 916 | 900 | 750 | 585 | 500 | 375 |
| Каратная система проб | 24 | 23 | 22 | 21,6 | 18 | 14 | 12 | 9 |
| Золотниковая система проб | 96 | 92 | 88 | 86,4 | 72 | 56 | 48 | 36 |
Сплавы с другими металлами
В промышленности применяются сплавы золота с медью, серебром, платиной, палладием, никелем и другими металлами. Лигатура меняет свойства сплава. Платина и палладий придают ему белый цвет, цинк и кадмий понижают температуру плавления (но цинк делает сплав хрупким, а кадмий — нет), медь окрашивает в красный и делает тверже.
Применение
Без золота нельзя представить себе:
- ювелирное дело,
- информационные технологии,
- нефтехимическое производство,
- производство измерительных приборов,
- элетронику и микроэлектронику,
- фармакологию,
- ядерные исследования.
До сих пор золото не утратило и первоначального предназначения — оно используется для сбережения и приумножения средств.
Как отличить подделку
Чтобы навариться, выдав изделия из неблагородных сплавов за ценные, мошенники прибегают к уловкам: обжигают серебро на огне, соединяют медь с цинком и оловом. Обращайте внимание на:
- Клеймо — оно должно соответствовать стандарту.
- Цену — если она неправдоподобно низка, это тревожный знак.
- Страну-производитель — проверьте украшение лишний раз, если это Турция, Китай или ОАЭ.
Встречаются советы попробовать вещь на зуб при продавце или испытать химически, капнув на нее йодом. Это действенные для определения подлинности высоких проб способы, но они не всегда приемлемы в обществе. Если продавец вызывает у вас сомнения настолько, что вы готовы кусать его товар, стоит отказаться от покупки.
Заключение
Не кладите золото в ртуть и не проливайте на него синильную кислоту — так оно прослужит дольше. А еще подписывайтесь на мои статьи и делитесь ими с друзьями!
Источник: xn—-ntbhhmr6g.xn--p1ai
Золото

Золото — химический элемент № 79, 11 группы (по устаревшей форме ПС — побочной подгруппы 1-ой группы), шестого периода периодической таблицы Д. И. Менделеева. Простое вещество золото — благородный металл жёлтого цвета.
Известно с древнейших времён, поскольку встречается в природе как свободный металл.
Золото выполняет функцию денег (всеобщий эквивалент и средство обеспечения национальной валюты). Используется в искусстве, ювелирном деле, медицине, сплавы золота — в технике (особенно в электронике как материал для контактов).
- 1 Происхождение
- 2 Изотопы
- 3 Физические свойства
- 4 Химические свойства
- 5 Нахождение в природе
- 6 Добыча золота
- 7 Применение
- 8 Получение золота
- 8.1 Промывание
- 8.2 Амальгамация
- 8.3 Цианирование
- 8.4 Регенерация
Происхождение
Золото в связи с его большим зарядом ядра не может образовываться при нуклеосинтезе внутри звёзд (в них реакции нуклеосинтеза протекают до образования самого стабильного изотопа железа-56). Предполагается, что оно может получаться при взрывах сверхновых и при столкновениях нейтронных звёзд.
Данные космические события редки, времени для создания золота немного, поэтому данного металла в природе очень мало.
Изотопы
Золото — моноизотопный элемент, в природе есть только 1 стабильный изотоп (золота-197). Из искусственно полученных радиоактивных изотопов золота наиболее важен Au-198. Из неустойчивых изотопов золота наибольший период полураспада имеет Au-195 (186 суток).
Физические свойства
Чистое золото — мягкий металл желтого цвета. Красноватый оттенок некоторым изделиям из золота, например, монетам, придают примеси других металлов, в частности, меди. В тонких пленках золото просвечивает зеленым или синевато-зеленым цветом.
Коллоидное золото может иметь красный и пурпурный цвет (т. н. кассиев пурпур).
Добавки серебра придают золоту зеленоватый оттенок, а меди — оранжевый или красноватый.
Белое золото — это его сплав с палладием.
Золото — мягкий металл, может царапаться ногтем и в чистом виде быстро истирается, поэтому его сплавляют с другими металлами (см. выше). Твёрдость по Моосу — 2,5; по Бриннелю 220—250 МПа.
Температура плавления золота: 1064 °C (1337 К), кипения — 2856 °C (3129 К). Плотность жидкого золота меньше, чем твердого, и составляет 17 г / см³ при температуре плавления. Жидкое золото довольно летучее, и активно испаряется задолго до температуры кипения.
Золото — тяжелый металл: плотность чистого золота — 19321 кг / м³ (шар из чистого золота диаметром 46 мм имеет массу 1 кг). Среди металлов по плотности занимает шестое место: после осмия, иридия, рения, платины и плутония. Высокая плотность золота облегчает его добычу. Самые простые технологические процессы, такие как промывка на шлюзах, могут обеспечить высокую степень извлечения золота из промывных пород.
Золото является высокопластичным металлом: оно может быть прокатано в пластинки толщиной до ~ 0,1 мкм (сусальное золото). Золото может быть вытянуто в проволоку с линейной плотностью до 500 м / ч.
Химические свойства

Растворение золота в царской водке
Золото — самый инертный металл, стоящий в ряду напряжений правее всех других металлов. При нормальных условиях оно не взаимодействует с большинством кислот и не образует оксидов, благодаря чему было отнесено к благородным металлам, в отличие от обычных металлов, которые разрушаются под действием окружающей среды. Затем была открыта способность царской водки растворять золото, что опровергло мнение о его химической инертности.
Наиболее устойчивая степень окисления золота в соединениях +3, в этой степени окисления оно легко образует с однозарядными анионами (F — , Cl — , CN — ) устойчивые плоские квадратные комплексы [AuX4] — . Относительно устойчивыми также являются соединения со степенью окисления +1, дающие линейные комплексы [AuX2] — . Долгое время существовало мнение, что +3 — высшая из возможных степеней окисления золота, однако, используя дифторид криптона, удалось получить соединения Au +5 (фторид AuF5, соли комплекса [AuF6] — ). Соединения золота (V) являются стабильными только со фтором; сильные окислители.
При взаимодействии атомарного фтора с пентафторидом золота были получены летучие фториды золота (VI) и (VII): AuF6 и AuF7. Они очень неустойчивы, особенно AuF6, который дисмутирует с образованием AuF5 и AuF7. [1]
Степень окисления +2 для золота несвойственно, в веществах, в которых она формально равна 2, половина золота, как правило, окисленный до +1, а половина — до +3, например, правильной ионной формулой сульфатов золота (II) AuSO4 будет не Au 2+ (SO4) 2- , а Au + Au 3+ (SO4) 2- 2, однако найденs комплексы, в которых золото все же имеет степень окисления +2.
Существуют соединения золота со степенью окисления −1, которые называются ауридами. Например, CsAu (аурид цезия). [2]
Нахождение в природе
Сразу после своего возникновения Земля была в расплавленном состоянии, и, поскольку золото — тяжёлый и инертный металл, то почти всё оно сейчас находится в земном ядре. Золото, которое сегодня присутствует в мантии и земной коре, в основном имеет астероидное происхождение, оно было доставлено на Землю во время поздней тяжелой бомбардировки 3,8-4,1 млрд лет назад.
Золото в природе находится преимущественно в самородном состоянии, в виде россыпей, или даже крупных кусков металла. Золото иногда встречается в виде природных сплавов с серебром, медью, висмутом, сурьмой, палладием, осмием, иридием, платиной.
К ним относятся электрум (природный сплав золота и 25 — 45 % серебра), порпесит AuPd, бисмутоаурит (Au, Bi); родистое золото, медистое золото, иридистое золото, платинистое золото, ауросмирид.
Немногочисленные минералы золота представлены в основном теллуридами: креннерит AuTe2, калаверит AuTe2, сильванит AuAgTe4, петцит Ag3AuTe2, мутманит (Ag, Au)Te, монтбрейит Au2Te3, нагиагит Pb5AuSbTe3S6.
Встречаются также минералы золота с селеном.
Оно также есть и в морской воде (около 5 кг золота в 1 кубическом километре воды).
Добыча золота

Как добывают золото [24:20]
Люди добывают золото с незапамятных времен. С золотом человечество столкнулось уже в V тыс. до н. э. в эпоху неолита благодаря его распространению в самородном состоянии.
По предположениям археологов, начало системной добычи было положено на Ближнем Востоке, откуда золотые украшения поставлялись, в частности, в Египет. Именно в Египте в гробнице королевы Зер и одной из королевы Пу-Оби Ур в Шумерской цивилизации были найдены первые золотые украшения, датированные III тыс. до н. э.
В России принято считать началом золотодобычи 21 мая (1 июня) 1745 г., когда Иерофей Марков, который нашел золото на Урале, объявил о своем открытии в Канцелярии Главного правления заводов в Екатеринбурге.
За всю историю человечеством добыто около 140 тыс. т. золота (если сплавить все это золото воедино, получится куб с размером одной стороны примерно 19 м).
В 2007 году добыли 2,38 тыс. т золота, а в 2008 — 2,33 тыс. т.
Применение

Золото в слитках
- Для запасов, в виде стандартных слитков чистого золота (чаще по 1 кг).
- Как средство вложения капитала.
- Производство золотых монет, медалей и т. д.
- В ювелирном деле.
- Некоторые соединения золота применяются в медицине.
- В электронике: микросхемы, контакты и т. п.
- Золотые припои, гальванические покрытия, золочение металлов.
- Золото зарегистрировано в качестве пищевой добавки Е175.
- Радиоактивное золото-198 используется при лечении злокачественных опухолей в радиотерапии.
- Лекарственные препараты (например миокризин, кризанин, солганал, санкризин).
- В ядерных реакциях, для производства некоторых изотопов франция (например франций-210).
Получение золота
Для получения золота используются его основные физические и химические свойства: присутствие в природе в самородном состоянии, способность реагировать только с немногими веществами (ртуть, цианиды). С развитием современных технологий более популярными становятся химические способы.
Промывание
Метод промывания базируется на высокой плотности золота, благодаря которой в потоке воды минералы со плотностью меньшей золота, а это почти все минералы земной коры, смываются, и металл концентрируется в тяжелой фракции песка, состоящего из минералов повышенной плотности (шлих). Этот процесс называется отмывкой шлиха либо шлихованием. В небольших объемах ее можно проводить вручную, при помощи промывочного лотка. Этот способ используется с древнейших времен, и до сих пор для обработки маленьких месторождений старателей, но основное его применение — поиск месторождений золота, алмазов и других ценных металлов.
Промывание используется для разработки крупных рассыпной месторождений, но при этом применяются специальные технические устройства: Драги и другие прамыцёвыя устройства. Полученные шлихи, кроме золота, содержат множество других плотных минералов и металл из них извлекается, например, путем амальгамации.
Методом промывания разрабатываются все россыпные месторождения золота, ограничено он используется на коренных месторождениях. Для этого породу дробят и затем подвергают промывания. Этот метод не может быть применен на месторождениях с рассеянным золотом, где оно так распылен в породе, что после измельчение не закрывается в отдельные зерна и смывается при прамыцьци вместе с другими минералов. К сожалению, при промывке теряется не только мелкое золото, но и крупные самородки.
Амальгамация
Цианирование
Согласно этому методу золото растворяется в растворах синильной закваски и ее солей, и это его свойство дало начало ряду методов добывания путем цианированию руд.
Метод цианирования основан на реакции золота с цианидом в присутствии кислорода от воздуха: измельченная золотоносных порода обрабатывается разведенным (0,3-0,03 %) раствором цианида, золото из образованного раствора цианоаурата Na[Au(CN)2] осаждается или цинковой пылью, либо на специальных ионообменных смолах.
Метод цианирования первоначально использовался на крупных заводах, где порода дробилась и цианирование проводилась в специальных чанах. Однако развитие технологии привело к появлению метода выщелочивания, который заключается в следующем: готовится водонепроницаемая площадка, на нее насыпается руда и ее обводняют растворами цианида, которые, просачиваясь через толщу породы, растворяют золото. После этого они поступают в специальные сорбционные колонны, в которых золото осаждается, а регенерированный раствор снова отправляется на свалку. Метод цианирования ограничен минеральным составом руд, он неприменим, если руда содержит большое количество сульфидов или арсенидов, так цианида реагируют с этими минералов. Поэтому цианированием перерабатываются малосульфидные руды или руды из зоны окисления, в которой сульфид и арсенид окислены атмосферным кислородом.
Для извлечения золота из сульфидных руд используются сложные многоэтапные технологии. Золото, добытое из месторождений, содержит различные примеси, поэтому его подвергают специальным процессам высокой очистки, изготавливаемые на аффинажных заводах.
Регенерация
Осуществляется действием 10 % раствором щёлочи на растворы солей золота с последующим осаждением аффинажного золота на алюминий.
Цены
В 2014 году средняя цена на золото составила $1267 за унцию (при том, что это значение в 2012 году составило $1669).
Биологическая роль
Золото не играет никакой биологической роли. Металлическое золото нетоксично. Некоторые растворимые соединения золота ядовиты.
Другие факты
- В 1947 годуамериканские физики Ингрем, Гесс и Гайдн получили 35 мкг золота в ходе эксперимента по измерению эффективного сечения поглощения нейтронов ядрами ртути. Золото получилось как побочный продукт. Таким образом, была осуществлена давняя мечта алхимиков, ртуть была превращена в золото. Однако данный способ не годится для промышленного получения золота — ведь такое золото будет несоизмеримо дороже, чем то, которое получают даже из самых бедных руд.
- Теоретически золото может быть получено путём бомбардировки природной ртути-196 нейтронами. Образующаяся радиоактивная ртуть-197 превращается в золото-197 путём бета-распада.
- Золото может быть вытянуто в проволоку длиной 1 км, но с массой всего 2 г.
- В Древней Руси золото сокращённо называлось «златом».
См. также
Источники
- ↑Химия и жизнь
- ↑ Неорганическая химия: в 3 т. / Под ред. Ю. Д. Третьякова. Т. 3: Химия переходных металлов. Кн. 2. М.: Изд. центр «Академия», 2007, 400 с.
Литература
- Баукова, Татьяна Валентиновна. Золото в химии и медицине. — М.: Знание, 1991. — 31 с: ил. — (Новое в жизни, науке, технике. Химия; 8/1991). — ISBN 5-07-002078-1
- Фосс, Г. В. Золото: типы месторождений, история добычи, сырьевые базы / Г. В. Фосс. — Москва: Госгеолтехиздат, 1963. — 174 с.
- Борисов, С. Н. Золото в современном мире / С. М. Борисов; РАН, Ин-т мировой экономики и междунар. отношений. — Москва: Наука, 2006. — 248 с.
- Белорусская энциклопедия: В 18 т. Т. 7 / Редкол.: Г. П. Пашков и др. — Минск: БелЭн, 1999. — 608 с .: ил
Ссылки
- Золото в Абсурдопедии на Викии (юмористическая статья)
Источник: cyclowiki.org