Коллоидное золото, издавна применяемое для лечебных целей, и сегодня под именем «нанозолота» активно используется в медицинской практике и в биомедицинских исследованиях. Однако механизм его терапевтического воздействия на организм до сих пор не установлен. Специалистам из Института химической биологии и фундаментальной медицины СО РАН (Новосибирск) впервые удалось проследить начальные этапы реального взаимодействия золотых наночастиц с клетками в условиях клеточной культуры и организма
Китайские, арабские и индийские ученые получали и использовали коллоидное золото в лечебных целях еще в V—IV вв. до н. э. В средние века его применяли многие врачи, включая знаменитого Парацельса, а алхимики пытались на его основе создать средство, возрождающее молодость и здоровье. В 1857 г. М. Фарадей опубликовал первую статью, посвященную методам синтеза и свойствам коллоидного золота, получившего в конце ХХ в. модную приставку «нано-». Последняя оказалась не просто лингвистическим довеском: взгляд на коллоидное золото, как на объект нанотехнологий, вызвал всплеск исследований, выявивших новые свойства давно известного металла и новые области его применения.
В организме каждого человека есть немного золота, однако…?
Сегодня благородный металл применяется в лечении ревматоидного артрита и других тяжелых аутоиммунных заболеваний, а также в медицинской диагностике в качестве контрастирующего агента. Новым перспективным направлением является использование золотых наночастиц как структурной основы нанокомпозитов, применяющихся для доставки в клетки молекул с лечебным эффектом.
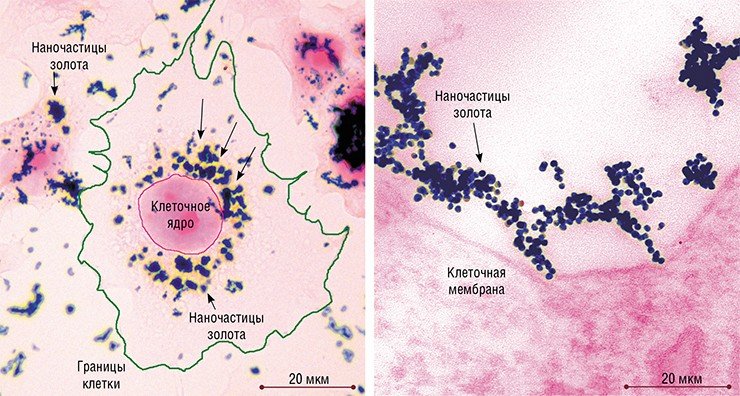
Во всех этих случаях наночастицы золота попадают внутрь организма человека и контактируют с клетками. Но безопасно ли «золотить» организм для борьбы с недугами? Чтобы не навредить пациенту, нужно знать, как наночастицы золота воздействуют на клетки, а для разработки препаратов адресной доставки необходимы сведения о путях проникновения наночастиц в клетку и их перемещении внутри клетки. Очень важен и вопрос о «судьбе» попавшего в клетки нанозолота. Как ни странно, ответы на эти вопросы нельзя найти среди тысяч современных публикаций, посвященных исследованиям этого материала.
Чтобы приблизиться к пониманию механизмов взаимодействия золотых наночастиц с клетками, исследователи из ИХБФМ СО РАН изучили проникновение сферических золотых наночастиц размером около 16 нм в клетки HeLa – широко применяемой культуры клеток человека, а также в клетки гепатомы А1 – опухоли, растущей непосредственно в перитонеальной полости мышей (клетки этой формы опухоли локализуются в асцитической жидкости свободно, не формируя плотных скоплений).
Внутри тебя есть золото — 10 удивительных фактов о твоем теле | Я знаю
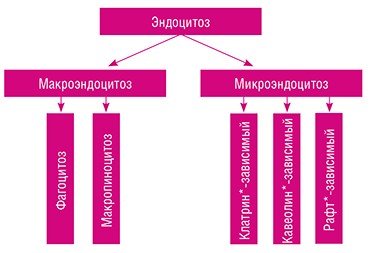
Наночастицы золота добавляли к питательной среде, в которой растут клетки культуры HeLa. При температуре 37 °С в них начинает работать так называемый эндоцитоз – процесс захвата клеткой веществ путем втягивания участка плазматической мембраны с последующим формированием внутри клетки пузырьков с внеклеточным содержимым. В зависимости от размеров формирующихся пузырьков говорят о макро- и микроэндоцитозе.
Макроэндоцитоз подразделяют на фагоцитоз, который обеспечивает поступление в клетку «твердых» частиц (обломков погибших клеток, бактерий), и макропиноцитоз, служащий для захвата относительно «больших» объемов внеклеточной жидкости.
Все виды микроэндоцитоза – клатрин-зависимый, кавеолин-зависимый и несколько видов рафт-зависимых * – «работают» с отдельными макромолекулами и их группами: захватывают их, сортируют и направляют в «нужное» место; этими же способами проникают в клетку и вирусы. Заканчивая краткий экскурс в терминологию, отметим, что проблемы эндоцитоза относятся к «горячим» направлениям современной биологии и сегодня активно разрабатываются, однако пока хорошо изучен лишь клатрин-зависимый тип эндоцитоза.
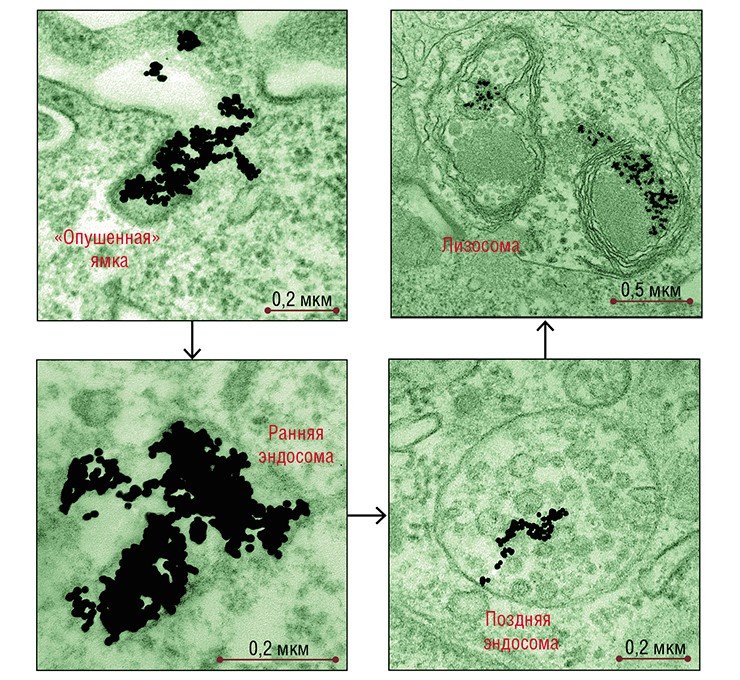
Что касается золотых наночастиц, то уже после 5 минут инкубации с клетками HeLa они обнаруживались в «опушенных» пузырьках и ямках – структурах, характерных для клатрин-зависимого эндоцитоза («опушение»образует белок клатрин). Через 30 минут количество «опушенных» структур достигало максимума, а потом постепенно снижалось.
В полном соответствии с «дорожной картой» клатрин-зависимого эндоцитоза наночастицы поступали на «сортировочную» станцию – в ранние, а затем в поздние эндосомы, сформированные мембраной округлые структуры с трубчатыми выростами. Эндосомы различаются набором ферментов и функциями: в ранних происходит сортировка макромолекул и частиц, а поздние расщепляют поступившие вещества с помощью гидролитических ферментов.
В клетках HeLa число поздних эндосом с наночастицами, как и количество самих наночастиц в них, нарастало в течение нескольких часов. Поздние эндосомы затем, как и положено, трансформировались в лизосомы, функцией которых является расщепление как поступивших извне веществ, так и «отработавших свое» собственных клеточных структур.
Однако клатрин-зависимый эндоцитоз обеспечивал поступление в клетки культуры HeLa лишь части золотых наночастиц. Еще часть попадала в клетку посредством схожего с ним кавеолин-зависимого эндоцитоза (кавеолы – фляжкоподобные углубления плазматической мембраны особого химического состава). Из кавеол наночастицы переносились посредством пузырьков в кавеосомы (аналоги ранней эндосомы), затем – в поздние эндосомы и т. д. Часть наночастиц попадала в клетку также путем рафт-зависимого эндоцитоза, о чем свидетельствовали редкие пузырьки соответствующей структуры у поверхности клеток.
Судя по данным световой микроскопии, ассоциаты наночастиц проникали в клетку и путем фагоцитоза, как другие крупные объекты. Однако тот факт, что через 2—3 суток инкубации основная масса наночастиц находилась в лизосомах или поздних эндосомах, свидетельствует, что основным путем их проникновения в клетки является все-таки микроэндоцитоз.
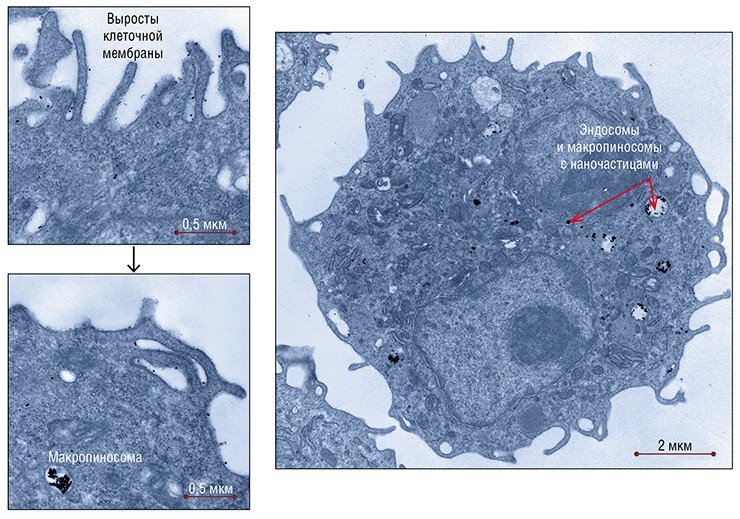
Процесс поглощения нанозолота клетками гепатомы А1 у лабораторных мышей отличался рядом особенностей. В основном наночастицы обнаруживались там в мелких пузырьках и трубочках, отражающих активные процессы рафт-зависимого эндоцитоза, а также в структурах, связанных с макроэндоцитозом – фагоцитозом и особенно макропиноцитозом, которые характерны для этих опухолевых клеток.
В процессе макропиноцитоза на поверхности клетки формируются длинные тонкие выросты-складки, которые смыкаются, захватывая все, что попадет внутрь. В результате образуется мембранный пузырь – макропиносома. Процессы утилизации веществ, поступивших в клетку путем макропиноцитоза, изучены слабо – априори считается, что макропиносомы впоследствии сливаются с лизосомами, без чего невозможна утилизация захваченных клеткой веществ. Несомненно лишь, что этот неспецифический путь поступления веществ не характерен для «нормальных» клеток организма, ведущих строгий «надзор» за поступающим в клетку материалом. Зато клетки опухоли с его помощью могут захватывать большие объемы жидкости, из которой они извлекают питательные вещества.
С течением времени проявления рафт-зависимого эндоцитоза в клетках гепатомы уменьшались, а основная масса наночастиц локализовалась в эндосомах и макропиносомах. И спустя несколько часов после введения наночастиц они продолжали оставаться в эндосомах, при этом трансформация последних в лизосомы не наблюдалась.
Судя по результатам этого исследования, разные типы клеток по-разному взаимодействуют с наночастицами золота. Некоторые ученые предполагают, что золотые наночастицы могут непосредственно связываться с клеточными рецепторами. Однако экспериментальные данные свидетельствуют скорее в пользу другой версии: что наночастицы попадают в клетку пассивно, вместе с другими поглощаемыми веществами, и теми путями, которые являются наиболее «естественными» для клеток данного типа.
В обоих случаях золотые наночастицы «застревали» в замкнутом пространстве эндосомально-лизосомальных структур, будучи изолированы от клеточной цитоплазмы непроницаемой мембранной оболочкой. Эти данные необходимо учитывать при конструировании комбинированных лечебных препаратов, так чтобы лечебная молекула могла отделяться от золотого «носителя» и попадать в цитоплазму клетки еще на стадии формирования ранних эндосом.
Конечно, пока ничего нельзя сказать о том, насколько прочной является эта мембранная «ограда», способна ли она удержать наночастицы до момента гибели клетки и не будут ли заключенные в лизосомы наночастицы провоцировать патологические реакции клеток? Поиск ответов на эти и другие далеко не «нановопросы» является предметом дальнейших исследований. Что же касается возможных практических приложений, то одному их них посвящен Интеграционный проект СО РАН № 9 «Разработка методов лазерного нагрева металлических наночастиц в биологических тканях для термического разрушения патологических клеток», в рамках которого была выполнена эта работа.
Д. б. н. Е. И. Рябчикова, к. х. н И. А. Пышная, Ю. Е. Спицына
(Институт химической биологии и фундаментальной медицины СО РАН, Новосибирск)
Дыкман Л. А., Хлебцов Н. Г. Золотые наночастицы в биологии и медицине: достижения последних лет и перспективы // ACTA NATURAE, 2011. Т. 3. № 2 (9). С. 36—59.
Chithrani D. B. Optimization of Bio-Nano Interface Using Gold Nanostructures as a Model Nanoparticle System // Insciences J. 2011. 1(3). P. 115—135.
Levy R., Shaheen U., Cesbron Y., See V. Gold nanoparticles delivery in mammalian live cells: a critical review // Nano Reviews. 2010. 1: 4889.
Sharma V., Park R., Srinivasarao M. Colloidal dispersion of gold nanorods: Historical background, optical properties, seed-mediated synthesis, shape separation and self-assembly // Materials Science and Engineering: R: 65 (2009). P. 1—38.
*Клатрин и кавеолин – белки, обеспечивающие изгибание плазматической мембраны и формирование пузырьков; рафты – скопления липидов в плазматической мембране, организованные особым образом
: 20 окт 2011 , Михаил Васильевич Ломоносов: «к приумножению пользы и славы Отечества» , том 40, №4
Источник: scfh.ru
Где находится золото в организме человека
Золото, уран и многое другое. Какие химические элементы можно обнаружить в человеческом организме? в текстах , фото , видео и аудио
Золото, уран и многое другое. Какие химические элементы можно обнаружить в человеческом организме?
24 июля 2019
Задумывались ли вы о том, что во время завтрака, чтения книги или по пути на учёбу в вашем организме функционирует настоящая химическая лаборатория? Если быть точнее – внутри нас и снаружи происходит множество химических реакций. Из курса школьной химии многим известно, что основу любой реакции составляют химические элементы, которых, кстати, в человеческом организме огромное количество. Но можно ли сказать, что человек полностью состоит из таблицы Менделеева? Миф это или реальность?
Начнём с простого. Организм человека в среднем состоит на 70 % из воды. Около 25 % приходится на органические вещества, которые состоят из углерода, водорода, кислорода, азота – четырёх химических элементов (так называемые «киты химии»). Они не только являются основными элементами жизни – из них состоят белки, вся природа вокруг нас и мы сами. К этим веществам также относят фосфор и серу.
Оставшаяся «масса» организма приходится на неорганические вещества – кальций, натрий, хлор, железо и другие элементы. В человеческом организме они существуют преимущественно в виде ионов (ионы – электрически заряженные частицы, возникающие при потере или присоединении электронов атомами, молекулами и радикалами. – Прим. автора) и поступают в него благодаря сбалансированному питанию и потребляемой воде.
Итак, присутствие некоторых элементов периодической таблицы Менделеева в нашем организме мы выявили. Но таблица Менделеева насчитывает свыше ста элементов. Где же остальные? Разобраться в этом вопросе поможет ассистент кафедры «Химия, химические процессы и технологии» Тольяттинского госуниверситета Сергей Соков.

Материал впервые опубликован в газете «Speechka» № 6 (114) от 25.04.2019 г.
Источник: talk-on.ru
Биосинтез и распад гемоглобина
Выпускник медицинского факультета УЛГУ. Интересы: современные медицинские технологии, открытия в области медицины, перспективы развития медицины в России и за рубежом.
- Запись опубликована: 12.08.2022
- Reading time: 3 минут чтения
Гемоглобин – это основной белок крови. Молекула гемоглобина, благодаря его уникальной части гем, связывает и отдает кислород, необходимый для нормальной работы всех органов и тканей в организме. Низкий уровень этого белка приводит к тяжелому состоянию — анемии, при котором нарушаются питание и правильная работа всех клеток организма. Избыток также опасен — молекулы железа окисляются и повреждают живые ткани.
Врачу, чтобы своевременно поставить правильный диагноз и применить правильную тактику лечения, очень важно знать и понимать все процессы, связанные с синтезом и распадом гемоглобина.
Что такое гемоглобин
Гемоглобин — сложный белок, осуществляющий перенос молекулярного кислорода от органов дыхания к тканям организма. Молекула гемоглобина состоит из глобина и гема.
Гем — комплексное соединение железа и протопорфирина IХ, состоящего из четырех пиррольных колец, соединенных СН-мостиками. Железо, находящееся в центре протопорфирина, связано с четырьмя атомами азота пиррольных колец двумя главными и двумя дополнительными связями. Одна из двух оставшихся связей используется для соединения с глобином, другая — с кислородом.
Глобин — тетрамер, образующийся в ретикулоцитах, и состоящий из двух пар полипептидных цепей. Он содержит 570 остатков 18 различных аминокислот, образующих полипептидные цепи, отдельные участки которых закручены в альфа-спирали, а сами полипептидные цепи свернуты в сферические компактные глобулы.
Биосинтез гемоглобина
Особенность синтеза этого соединения — синхронное образование гема и глобина. Затем эти вещества соединяются в ретикулоцитах, образуя гемоглобин. Механизм позволяет синтезировать строго одинаковое количество обоих элементов.
Гем регулирует синтез глобина: при снижении скорости синтеза гема синтез глобина в ретикулоцитах тормозится. Процесс регулируется веществами 5-аминолевулинатсинтазой и аминолевулинатдегидратазой. В ретикулоцитах синтез фермента регулирует железо.
Нарушение синтеза гемоглобина, приводит к порфирии – заболеванию, при котором в гепатоцитах, нормобластах и эритроцитах накапливается излишек порфирина.
Образование порфибриногена
Гем синтезируется практически во многих клеточных структурах, но с наибольшей скоростью он вырабатывается в печени и костном мозге. Железо, необходимое для его и синтеза, поступает в организм с пищей и из разрушенных «старых» эритроцитов. При его нехватке синтез гема, а в дальнейшем, гемоглобина, замедляется и у человека возникает анемия.
- Образование 5–аминолевулиновой кислоты (5–АЛК). Вещество образуется из тиоэфира дикарбоновой янтарной кислоты и кофермента А – (сукцинила – КоА) и глицина в матриксе митохондрий. Катализатором выступает 5-аминолевулинатсинтаза – пиридоксальфосфат- зависимый фермент. Он служит регулятором протекания реакции.
- Образование порфобилиногена. Из митохондрий 5-АЛК поступает в цитоплазму, где ее молекулы соединяются по две, образуя моно- порфобилиноген, имеющий пиррольное кольцо и две молекулы воды. Реакция проходит в присутствии. аминолевулинат-дегидратазы – фермента, локализованного в жидком содержимом клетки – цитозоле
- Образование гидроксиметилбилана. Вещество образуется из четырех молекул порфобилиногена с образованием линейного тетрапиррола — гидроксиметилбилана. Катализатором служит фермент порфобилиноген-дезаминаза.
Окончательное образование гема
Вначале из гидроксиметилбилана образуется уропорфириноген III. Катализатором процесса служит вещество уропорфириноген III-косинтаза. Затем из уропорфириногена удаляются четыре карбоксильных группы с образованием копропорфириногена. Катализирует процесс фермент уропорфириноген-декарбоксилаза
После этого Урофибриноген III превращается в присутствии фермента уропорфириноген-декарбоксилазы в Копрофибриноген III.
После чего процесс опять переходит в митохондрии, где тем Копрофибриноген III превращается в протопорфириноген IX с помощью фермента копропорфириноген-оксидазы, а затем под воздействием протопорфириноген-оксидазы – в Протопорфирин -IX.
На заключительно этапе синтеза гема фермент феррохелатаза, присоединяет к протопорфирину IX двухвалентное железо.
Образование глобина
Цепи глобина синтезируются на полисомах, образованных пятью рибосомами. Цепь а освобождается первой, присоединяется к р-цепи, еще связанной с рибосомой, и отделяет ее, образуя димер (аР). Два димера соединяются в молекулу НЬ (а2Р2).
Синтез цепей глобина идет на полирибосомах и контролируется генами 11 и 16 хромосом. Гены, контролирующие синтез α- цепи, находятся одной хромосоме, а отвечающие за синтез β-, γ-, δ- и ε-цепи- в другой. У взрослого человека глобин состоит из двух а- и двух Р- полипептидных цепей.
Образование гемоглобина
После образования гем и глобин соединяются в единое вещество – гемоглобин. Это вещество связывает кислород, обеспечивая клеточное дыхание. Зрелые расные кровяные тела, образующиеся из ретиекулоцитов, на 85% заполнены гемоглобином. Каждый эритроцит содержит около 400 млн. молекул этого вещества. Всего в гемоглобине имеются четыре участка связывания кислорода (по одному гему на каждую субъединицу), то есть одновременно может захватывать четыре кислородные молекулы.
Гемоглобин у взрослых людей, имеющий две а- и две Р-цепи глобина, называется А-типом (от adult — взрослый). На него приходится 98% объема этого кровяного элемента. Но в крови обнаруживаются и вариации этого вещества с немного измененной структурой глобина, на которые приходится 2% этого вещества. Их роль до конца не изучена.
Распад гемоглобина
Красные кровяные тельца – эритроциты, в которых содердится гемоглобин, живут примерно 120 дней, после чего распадаются. В сновном этот процесс происходит в селезенке, но часть телец разрушается в печени и костном мозге.
10-20% эритроцитов разрушается при внутрисосудистом гемолизе. Их гемоглобин освобождается непосредственно в плазму, где связывается плазменным белком — гаптоглобином. Это гликопротеин, при электрофорезе белков мигрирующий с а2— глобулином. Половина объема образовавшегося комплекса — гемоглобин-гаптоглобин за 10 минут покидает плазму и поглощается паренхиматозными клетками печени, что предупреждает поступление свободного гемоглобина в почки.
В остальных случаях распад гемоглобина начинается с разрыва α-метиновой связи между I и II кольцами порфиринового кольца. Катализатором процесса выступает НАДФ-содержащая оксидаза. В первой стадии разложения гемоглобина уваствуют витамин С, ионы двухвалентного железа и другие кофакторы. Гемоглобин превращается в вердоглобин, меняя цвет с красного на зеленый.
Дальнейший распад проходит с освобождением железа, белка-глобина и образованием одного из желчных пигментов — биливердина. Освободившееся железо используется для образования нового гемоглобина. Для этого белок-ферритин переносит его в печень, где находится депо железа. Белки распадаются до аминокислот и используются для повторного белкового синтеза.
Образовавшийся биливердин ферментативным путем при помощи белка-редуктазы превращается в печени в билирубин, являющийся основным желчным пигментом. Это вещество, имеющее жетоватый цвет, необходимо для производства желчи. При массовом распаде кровяных клеток и освобожении большого количества гемоглобина у больного резко возрастает уровень биллирубина в крови и возникает желтуха.
Билирубин, образовавшийся в клетках ретикулоэндотелия, называется свободным, поскольку из-за плохой растворимости в воде он легко адсорбируется на белках плазмы.
Несвободный, или конъюгированный, составляющий комплекс билирубина с глюкуроновой кислотой, попадает по системе желчных протоков в кишечник, где конъюгат билирубина расщепляется β-глюкуронидазой, Освободившийся желчный фермент постепенно восстанавливается до бесцветного уробилиногена и стеркобилиногена, которые окисляются кислородом воздуха до уробилина и стеркобилина.
При прекращении процесса, например, при гепатите кал становится светдым «собачьим», а моча — темной. Это значит, что биллирубин перестал поступать в кишечник, а начал впитываться в кровь, выделяясь с мочой.
Механизм бактериальных превращений билирубина до стеркобилиногена и стерокобилина еще не до конца расшифрован. Имеются данные, что промежуточными продуктами процесса яляются мезобилирубин и уробилиноген. После всасывания небольшая часть мезобилиногена поступает через воротную вену в печень, где подвергается разрушению с образованием моно- и дипиррольных соединений.
Выводы
Каждому врачу следует знать схему распада молекулы гемоглобина, так как в норме в крови содержится определенное количество желчных пигментов. При развитии патологических процессов в печени и селезенке, показатели билирубина значительно повышаются. Такое поражение может привести к развитию печеночной комы и летальному исходу.
Не менее важно понимать процесс синтеза гемоглобина. Зная этот механизм, можно понять причины анемии и успешно ее лечить.
Источники
- Биохимия: Учеб. для вузов. Под ред. Е.С. Северина, 2003.
- Электронное издание на основе: Биологическая химия с упражнениями и задачами: учебник под ред. чл.-корр. РАМН С.Е. Северина, 2011.
- ФБУ ВО УГМУ Минздрава Росии Гаврилов И.В. Лекция 17 «Биохимия лейкоцитов, гемоблобина и эритроцитов», 2016 г.
- Папаян А. В., Жукова Л. Ю. Анемии у детей, 2001.
- Степанов В.М. Молекулярная биология. Структура и функция белков, 1996.
- Т.Т.Березов, Б.Ф.Коровкин «Биологическая химия», 1998 г.
- Большая Медицинская Энциклопедия (БМЭ), под редакцией Петровского Б.В., т. 5 3-е издание.
- Ленинджер А. «Основы биохимии», 1985.
Источник: unclinic.ru











