От слова «валентность» многие ученики, изучающие химию в 8 классе, впадают в спячку. В школьном курсе химии этому вопросу уделяется не так много времени, хотя валентность – одно их базовых понятий в этой науке. Очень важно досконально разобраться, что такое валентность , как она определяется и какое значение она имеет. Поняв это и научившись составлять формулы и определять валентность элементов, вы существенно облегчите себе изучение химии. Приступаем.
Фото: pixabay.com
Что же такое валентность? Ничего страшного в этом явлении нет.
Валентность – это способность атома образовывать химические связи.
Вы же знаете, что бывают вещества простые, состоящие из атомов одного вида, и сложные, состоящие из атомов разных элементов? Так вот чтобы атомы как-то соединялись между собой, они должны связываться, соединяться. А соединяются они посредством химической связи . Одни атомы могут образовать только одну связь, на большее у них способностей не хватает.
Валентность. Учимся определять валентность элементов по формулам
Другие атомы куда мощнее, они могут и несколько связей образовать, чтобы покрепче держаться за окружение. Вот представьте, что у вас только один друг. Надёжный такой, верный друг, который с вами в огонь и в воду. Вы с ним всегда в паре ходите. Это значит, что у вас валентность I (внимание!
Читается это не «первая валентность», а «валентность один»!). А теперь представьте, что у вас три верных друга. Вы всегда за них держитесь и твёрдо уверены, что они при вас ежеминутно. Значит, у вас валентность III. В первом случае вы образовали одну крепкую связь, а во втором – три.
Вот и вся валентность.
Любой учитель и репетитор по химии скажет вам, что
есть элементы с валентностью постоянной и элементы, у которых валентность может быть разной.
И, как ни странно, они будут правы. Если мы возвратимся к примерам с друзьями, то выглядеть это будет так. Кто-то всю жизнь дружит с одним человеком (у него всегда валентность I), кто-то всю жизнь дружит с тремя (валентность III). А кто-то иногда дружит с одним, иногда с тремя, а иногда — вообще с пятью! Встречали таких в жизни?
Вот и среди химических элементов есть такие, которые иногда имеют валентность I, иногда валентность III или даже V. Должна вас немного расстроить: элементы с постоянной валентностью придётся зазубрить . Также навсегда запоминаем, что валентность обозначается римскими цифрами (так повелось, просто смиритесь с этим. Указывается валентность НАД элементом в формуле). Итак, наизусть нужно выучить, что:
· Металлы основной подгруппы первой группы всегда имеют валентность I. Это элементы Li, Na, K, Rb, Cs, Fr.
· Металлы основной подгруппы второй группы всегда имеют валентность II. Это элементы Be, Mg, Ca, Sr, Ba, Ra.
· Водород всегда имеет валентность I.
· Кислород всегда имеет валентность II.
· Элементы Al и В (основная группа третьей подгруппы) всегда имеют валентность III.
· Элементы основной подгруппы седьмой группы чаще (но не всегда!) имеют валентность I. Это элементы F, Cl, Br, I, At. Кстати, эти элементы носят название «галогены» и будьте настороже: галогены любят подшутить и иногда имеют другую валентность. В школьной химии обычно они представляются как одновалентные, но это кокетство, потому что галогены – шалуны.
Как БЫСТРО определить ВАЛЕНТНОСТЬ #shorts #youtubeshorts
Теперь перейдём к элементам с валентностью непостоянной. Это хулиганы, которые любят загадывать загадки и разыгрывать начинающих. Особое коварство они проявляют во время ЕГЭ по химии и даже ОГЭ по химии, запутывая бедных школьников. Итак,
запомните этих головорезов с непостоянной валентностью в лицо:
C (углерод), N (азот), P (фосфор), S (сера), Сr (хром), Fe (железо), Cu (медь).
Конечно же, в таблице Менделеева элементов намного больше. Но в школьном учебнике по химии используется менее половины из них. Дело в том, что в четвёртом периоде таблицы появляются так называемые d-элементы со сложным строением и хитрыми свойствами, о которых школьникам рассказывать не полагается. Да и очень хорошо, нечего голову забивать.
Надеюсь, с понятием «валентность» вы всё-таки разобрались. В следующий раз мы попрактикуемся в определении валентности элементов, если есть формула, и правильном составлении формул веществ, если знаем валентность.
Пишите, пожалуйста, в комментариях, что осталось непонятным, и я обязательно дам дополнительные пояснения. Жалуйтесь на сложности в изучении школьного курса и говорите, что вас испугало в учебнике химии. И тогда следующая статья будет рассказывать именно об этой проблеме.
Источник: dzen.ru
Как определить валентность золота
Валентность химических элементов – это способность у атомов химических элементов образовывать некоторое число химических связей. Определяется числом электронов атома затраченых на образование химических связей с другим атомом.
Считается, что валентность химических элементов определяется группой (колонкой) Периодической таблицы . Действительно, теоретически, это самая распространенная валентность для элемента, но на практике поведение химических элементов значительно сложнее. Причина множественности значений валентности заключается в том, что существуют различные способы (или варианты) заполнения, при которых электронные оболочки стабилизируются. Поэтому, предлагаем Вашему вниманию таблицу валентностей химических элементов.
Числовое значение положительной валентности элемента равно числу отданных атомом электронов, а отрицательной валентности – числу электронов, которые атом должен присоединить для завершения внешнего энергетического уровня. В неорганической химии обычно применяется понятие степень окисления, а в органической химии — валентность, так как многие из неорганических веществ имеют немолекулярное строение, а органических — молекулярное..
Порядковый номер
химического элемента,
он же: атомный номер,
он же: зарядовое число
атомного ядра,
он же: атомное число
Русское /
Английское наименование
Химический
символ
Валентность
В скобках обозначены
более редкие валентности.
Химические элементы с
единственной валентностью
— одну и имеют.
Источник: dpva.ru
Валентность
Из этой статьи вы узнаете, что называется валентностью в химии, научитесь находить ее значение и использовать для составления химических формул.
· Обновлено 23 июня 2023
Понятие валентности
Валентность — это способность атома химического элемента образовывать определенное число химических связей с другими атомами.
Рассмотрим структурную формулу H2SO4, с помощью которой можно определить, как атомы связаны между собой в веществе:
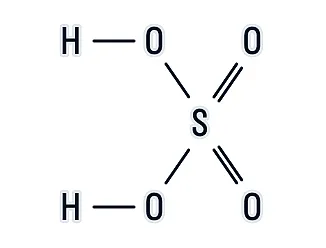
Исходя из структуры, можно сделать выводы:
- атомы водорода H имеют одну химическую связь, то есть одновалентны;
- сера S имеет шесть химических связей, то есть шестивалентна;
- каждый атом кислорода O имеет две химические связи — двухвалентен.
Валентность обозначается римской цифрой над знаком химического элемента в формуле. Например:

Атом натрия имеет валентность, равную 1, а атом кислорода — равную 2.
Получай лайфхаки, статьи, видео и чек-листы по обучению на почту
![]()
Полезные подарки для родителей
В колесе фортуны — гарантированные призы, которые помогут наладить учебный процесс и выстроить отношения с ребёнком!
Получить подарок!
Постоянная и переменная валентность
Среди всех элементов выделяют две группы: с постоянной и переменной валентностью.
У элементов с постоянной валентностью в любом соединении она одинакова. Эти элементы и проявляемую ими валентность придется выучить.
O, Be, Mg, Ca, Ba, Zn
Переменная валентность меняется в зависимости от соединения. Элементов с переменной валентностью большинство. Как правило, они характеризуются высшей, промежуточной и низшей валентностью:
- высшая валентность для элементов главных подгрупп совпадает с номером группы (№гр);
- низшая валентность вычисляется по формуле: 8 − №гр;
- промежуточная валентность — число между низшей и высшей валентностью. Обычно промежуточные валентности соответствуют четности группы.
Пример: как определить валентность по таблице Менделеева
Сера S располагается в группе VIА таблицы Менделеева. Значит:
- высшая валентность серы равна VI;
- вычислим низшую валентность: 8 − 6 = 2. Низшая валентность равна II;
- сера расположена в группе VI — это четное число. Значит, промежуточными валентностями будут все четные числа между низшей и высшей валентностью. В случае с серой между числами 2 и 6 расположено только одно четное число — 4. Промежуточная валентность серы — IV.
В таблице собрали все возможные валентности для некоторых химических элементов.
Обратите внимание
Понятия «степень окисления» и «валентность» — это не одно и то же, хотя в большинстве случаев они численно совпадают. Степень окисления — это условный заряд атома, он бывает положительным или отрицательным. А валентность — способность атома образовывать связи, она не может принимать отрицательные значения.
Как определить валентность химического элемента с переменной валентностью в соединении
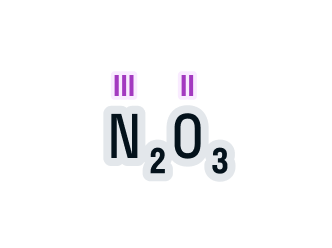
Определим валентность азота в соединении N2O3.
- Над элементами с постоянной валентностью подпишем ее значение, в нашем случае это кислород:
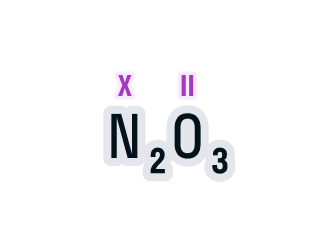
- Общее число валентностей каждого элемента в соединении должно совпадать. Находится общее число валентностей с помощью умножения валентности на число атомов данного химического элемента в соединении. Считаем: общее число валентностей кислорода равно 2 · 3. Значит, общее число валентностей азота в данном соединении будет равно x · 2. Получаем уравнение: х · 2 = 2 · 3.
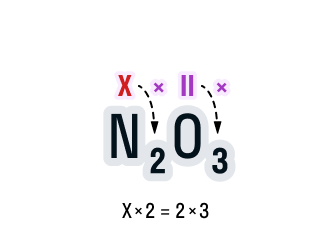
- Вычислим х в получившемся уравнении: 2х = 6; х = 3.
- Валентность азота в данном химическом соединении равна трем.
 Встречаются бинарные соединения (то есть соединения, состоящие только из двух видов атомов), в которых неизвестны валентности обоих атомов элементов. Как найти валентности химических элементов в этом случае? Для определения значения валентности необходимо запомнить, что неметаллы в бинарных соединениях, расположенные на втором месте, проявляют свою низшую валентность. Например, в сульфидах (FeS) сера расположена на втором месте и проявляет низшую валентность, равную двум. Тогда валентность железа в данном сульфиде можно рассчитать по приведенному выше алгоритму — ее значение равно двум.
Встречаются бинарные соединения (то есть соединения, состоящие только из двух видов атомов), в которых неизвестны валентности обоих атомов элементов. Как найти валентности химических элементов в этом случае? Для определения значения валентности необходимо запомнить, что неметаллы в бинарных соединениях, расположенные на втором месте, проявляют свою низшую валентность. Например, в сульфидах (FeS) сера расположена на втором месте и проявляет низшую валентность, равную двум. Тогда валентность железа в данном сульфиде можно рассчитать по приведенному выше алгоритму — ее значение равно двум.  В хлоридах (например, AgCl) хлор проявляет низшую валентность, равную единице.
В хлоридах (например, AgCl) хлор проявляет низшую валентность, равную единице.
Как составить формулу химического соединения по значениям валентностей элементов
Составим формулу оксида фосфора (V).
- Записываем обозначения элементов и над ними указываем валентности. Валентность фосфора в данном соединении указана в названии вещества (V), а валентность кислорода всегда равна II.

- Находим НОК валентностей, в нашем случае 5 · 2 = 10. Для удобства запишем его над формулой:

- Делим НОК на валентность каждого элемента, а результат записываем в индекс: 10 : 5 = 2 — индекс фосфора; 10 : 2 = 5 — индекс кислорода.
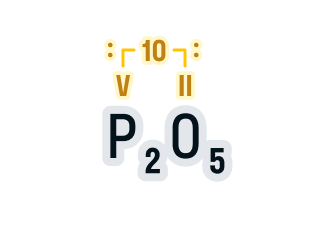 Получаем соединение P2O5.
Получаем соединение P2O5.
Вопросы для самопроверки
- Что такое валентность в химии? Можно ли сказать, что валентность и степень окисления — это одно и то же?
- Как узнать высшую и низшую валентность какого-либо химического элемента?
- Назовите три химических элемента с валентностью, равной единице.
- Среди перечисленных химических элементов выберите те, у которых валентность переменная: K, S, Al, Cu, Ca, P, Si, Mn, Mg, O.
- Определите значения валентностей каждого химического элемента в следующих соединениях: FeCl3, Cl2O7, CuS, AlP.
- Составьте химические формулы веществ:
- Хлорид железа (II).
- Оксид углерода (IV).
- Оксид магния.
- Верно ли, что значение высшей валентности химических элементов увеличивается по периоду слева направо в таблице Менделеева?
Тему «Валентность» проходят на уроках химии в 8-м классе, и без ее понимания сложно двигаться дальше, а уж тем более сдавать государственные экзамены. Онлайн-курс подготовки к ЕГЭ по химии от Skysmart поможет освежить знания за все годы школьной программы, заполнить пробелы и снять стресс перед экзаменом. Вводный урок бесплатный!
Источник: skysmart.ru