Найдите правильный ответ на вопрос ✅ «Найдите энергию связи золота . » по предмету Физика, а если вы сомневаетесь в правильности ответов или ответ отсутствует, то попробуйте воспользоваться умным поиском на сайте и найти ответы на похожие вопросы.
Новые вопросы по физике
Проводники сообщили заряд 1*10’9 кл, его зарядили до потенциала 100 в. Определить электроемкость проводника?
Две стальные проволоки, имеющие одинаковые длины, но разные сечения, включены параллельно в цепь. В какой из них будет выделяться большее количество теплоты за одно и то же время?
Что определяется выражением Q/m
Скорость автобуса равна20 м/с а скорость гоночного автомобиля 360 км/ч. Во сколька раз скорость гоночного автомобиля больше скорости автобуса
Источник: iotvet.com
Какой тип связи у золота
Привет Лёва Середнячок

Е100 3 Отметки 2 ч | Розыгрыш Золота | Стрим Мир танков
Какой тип кристаллической решетки характерен для следующих веществ: хлорид калия, графит, сахар, йод, сульфид натрия, Na2S,золото и кремнизем, и вид химической связи
Ответ проверен экспертом
4 (20 оценок)
himichka1974 9 лет назад
Светило науки — 84 ответа — 1058 раз оказано помощи
хлорид калия и сульфид натрия — ионная кристаллическая решетка — ионная связь
сахар, йод — молекулярная крист. решетка — ковалентная полярная и неполярная связь
золото — металлическая кристаллическая решетка — металлическая связь
графит, кремнезем — атомная кристаллическая решетка — связь ковалентная неполярная и полярная
Источник: vashurok.com
Металлическая химическая связь

Металлическая связь образуется между атомами в кристалле металла, возникающая за счет перекрытия валентных электронов. Так, что же представляет собой этот вид связи, и в каких соединениях она присутствует?
Что такое металлическая связь?
Металлическая химическая связь существует в металлическом кристалле и в жидком расплавленном состоянии. Ее образуют элементы, атомы которых на внешнем уровне имеют мало электронов (1-3) по сравнению с общим числом внешних, энергетически близких орбиталей.

Валентные электроны из-за небольшой энергии ионизации слабо удерживаются в атоме. Так, у атома натрия на один валентный электрон (3S1) приходится 9 свободных и энергетически близких орбиталей (одна 3s, три 3p и пять 3d).
Из-за малого значения энергии ионизации валентный электрон слабо удерживается и свободно перемещается не только в пределах 9 своих свободных орбиталей, но при плотной упаковке в кристалле и на свободных орбиталях других атомов, осуществляя связь.
ЗОЛОТО 99,9% ИЗ СОТНИ РАЗЛИЧНЫХ КОНТАКТОВ!
Химическая связь сильно делокализована: электроны обобществлены («электронный газ») и перемещаются по всему куску металла, в целом электронейтрального, между положительно заряженными ионами.
Свободное перемещение электронов по кристаллу объясняет ненаправленность и ненасыщенность связи, а также такие физические свойства металлов, как пластичность, блеск, электро- и теплопроводность.
Характерные кристаллические решетки
Металлы почти всегда образуют высокосимметричные решетки с плотно приближенными друг к другу атомами. Выделяют три вида кристаллических решеток:
- кубическая объемно центрированная. В таком виде решетки атомы располагаются на вершине куба и один атом в центре объема куба. Такую решетку имеют следующие металлы: натрий, литий, барий, калий, свинец и многие другие.
- кубическая гранецентрированная.
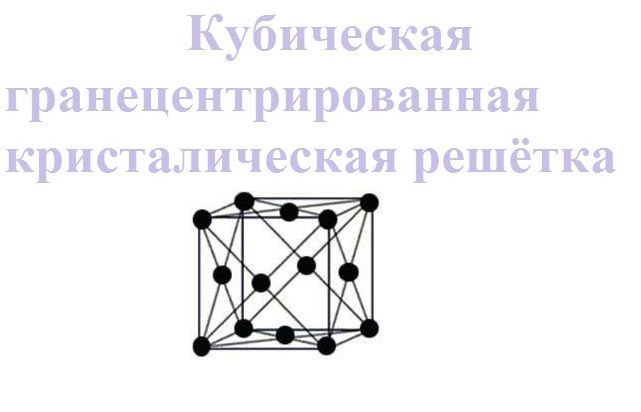
В таком виде решетки атомы располагаются в вершине куба и в центре каждой грани. Такой тип решетки имеют следующие металлы: церий, стронций, никель, серебро, золото, палладий, платина, медь и многие другие.
- гексагональная. В таком виде решетки атомы располагаются в вершине и центрах шестигранной оснований призмы, а три атома находятся в средней плоскости этой призмы.
Такой тип кристаллической решетки имеют следующие металлы: магний, кадмий, рений, осмий, рутений, бериллий и многие другие.
Что мы узнали?
Металлическая связь близка по природе к ковалентной, но отличается от нее тем, что обобществление электронов при ее образовании осуществляется сразу многими атомами. В данной статье дается определение понятию «металлическая связь», а также приведены примеры металлической химической связи.
Источник: obrazovaka.ru