Впервые спектральные линии поглощения атомов были обнаружены при изучении спектра Солнца в начале XIX века английским врачом и химиком Уильямом Волластоном, а затем и немецким физиком Иосифом Фраунгофером. Связь между видами спектров атомного поглощения и испускания и химическим составом нагретого газа была установлена немецкими учёными Робертом Бунзеном и Густавом Кирхгофом в 1859—1861 годах. С того времени спектры испускания (эмиссии) атомов стали широко применять в качественном и количественном определении элементов ПСХЭ в пробах разного состава и агрегатного состояния. Спектры поглощения (абсорбции) атомов в аналитических целях стали применять с 1930—1940-х годов для идентификации некоторых элементов в атмосферах звёзд, а также для определения содержания ртути в различных пробах и атмосфере помещений, однако они не были широко распространены в связи с тем, что отсутствовала удобная и высокочувствительная схема измерения.
В 1955 году британско-австралийский физик Алан Уолш[en] предложил простой и легко осуществимый на практике способ количественного определения содержания элементов в растворах, распыляемых в пламя ацетилен—воздух, по поглощению излучения атомных линий от специальных селективных ламп. Этот способ, лежащий в основе аналитического метода атомно-абсорбционной спектрометрии, предопределил развитие метода в дальнейшем. В 1962 году основанная Уолшем фирма Techtron[en] выпустила первый в мире серийный атомно-абсорбционный спектрометр АА-2. В качестве атомизатора вначале служило пламя, однако в 1960-х годах Борис Львов и Ганс Массман предложили использовать графитовую печь, которые для ААС впоследствии стали производить в промышленности.
Полевой метод определения золота в рудах. Проверка метода
Атомно-абсорбционная спектрофотометрия (ААС) – это современный, широко используемый метод определения элементного состава вещества по атомным спектрам поглощения.
Переход в атомное состояние происходит при распылении раствора пробы в высокотемпературное пламя, которое получают при горении ацетилена в воздухе или кислороде. Температура пламени в воздухе — 1900ºС, в кислороде — 3100ºС. Через пламя пропускают излучение определенной для каждого химического элемента длины волны. Для этого используют специальные лампы, испускающие очень узкий пучок света известной интенсивности. Часть излучения поглощается химическим элементом, находящимся в пламени; интенсивность прошедшего света замеряется с помощью фотоэлементов.
2. Экспресс определение ртути в почвах
Ртуть и многие её соединения ядовиты. Воздействие ртути — даже в небольших количествах — может вызывать серьёзные проблемы со здоровьем и представляет угрозу для внутриутробного развития плода и развития ребёнка на ранних стадиях жизни. Ртуть может оказывать токсическое воздействие на нервную, пищеварительную и иммунную системы, а также на легкие, почки, кожу и глаза. ВОЗ рассматривает ртуть в качестве одного из десяти основных химических веществ или групп химических веществ, представляющих значительную проблему для общественного здравоохранения.
КАК ОПРЕДЕЛИТЬ ЗОЛОТО В РУДАХ БЕЗ КИСЛОТ!? ЭТО НЕ ЙОД И ЗЕЛЁНКА…!)
Наиболее ядовиты пары́ и растворимые соединения ртути. Сама металлическая ртуть менее опасна, однако она постепенно испаряется даже при комнатной температуре. Пары могут вызвать тяжёлое отравление, для чего достаточно, например, ртути из одного разбитого медицинского термометра.
Ртуть и её соединения (сулема, каломель, киноварь, цианид ртути) поражают нервную систему, печень, почки, желудочно-кишечный тракт, при вдыхании — дыхательные пути (а проникновение ртути в организм чаще происходит именно при вдыхании её паров, не имеющих запаха). По классу опасности ртуть относится к первому классу (чрезвычайно опасное химическое вещество). Опасный загрязнитель окружающей среды, особенно опасны выбросы в воду, поскольку в результате деятельности населяющих дно микроорганизмов происходит образование растворимой в воде и токсичной метилртути, накапливающейся в рыбе. Ртуть — типичный представитель кумулятивных ядов.
Органические соединения ртути (диметилртуть и др.) в целом намного токсичнее, чем неорганические, прежде всего из-за их липофильности и способности более эффективно взаимодействовать с элементами ферментативных систем организма.
Болезнь Минаматы — синдром, вызываемый отравлением органическими соединениями ртути, преимущественно метилртутью. Была впервые обнаружена в Японии, в префектуре Кумамото в городе Минамата в 1956 году. Симптомы включают нарушение моторики, парестезию в конечностях, ухудшение внятности речи, ослабление зрения и слуха, а в тяжёлых случаях — паралич и нарушение сознания, завершающиеся летальным исходом.
Гигиеническое нормирование концентраций ртути. Предельно допустимые уровни загрязнённости металлической ртутью и её парами:
ПДК в населённых пунктах (среднесуточная) — 0,0003 мг/м³
ПДК в жилых помещениях (среднесуточная) — 0,0003 мг/м³
ПДК воздуха в рабочей зоне (макс. разовая) — 0,01 мг/м³
ПДК воздуха в рабочей зоне (среднесменная) — 0,005 мг/м³
ПДК сточных вод (для неорганических соединений в пересчёте на двухвалентную ртуть) — 0,005 мг/л
ПДК водных объектов хозяйственно-питьевого и культурного водопользования, в воде водоёмов — 0,0005 мг/л
ПДК рыбохозяйственных водоёмов — 0,00001 мг/л
ПДК морских водоёмов — 0,0001 мг/л
Демеркуризация. Очистка помещений и предметов от загрязнений металлической ртутью и источников ртутных паров называется демеркуризацией. В быту самой частой ситуацией для демеркуризации является ртуть, вылившаяся из разбитого ртутного термометра, что не представляет серьёзной опасности, но требует аккуратности и соблюдения правил безопасности.
Необходимо аккуратно собрать все раскатившиеся шарики ртути (например, сложить на влажное бумажное полотенце, собирать удобно пипеткой, можно кисточкой, можно широким скотчем), нужно внимательно осмотреть самые дальние углы комнаты. Затем сложите всё, что касалось ртути, в пакет с молнией и закройте его, положите в другой пакет с молнией и его тоже закройте (на случай, если один из них порвётся), после чего позвоните по номеру 112 в единую дежурную диспетчерскую службу и выясните, куда нужно сдавать собранную ртуть, и сдайте её на переработку. Также необходимо будет проветрить помещение в течение суток (открыть окна). Выбрасывать ртуть в бытовой мусор или сливать в канализацию нельзя. Также нельзя использовать пылесос для сбора ртути — он разобьёт ртуть на мельчайшие капли и ускорит её испарение, тем самым концентрация паров ртути повысится вплоть до опасного уровня.
С 2020 года международная конвенция, названная в память массового отравления ртутью и подписанная многими странами, запретил производство, экспорт и импорт нескольких различных видов ртутьсодержащих продуктов, применяемых в быту, в том числе электрических батарей, электрических выключателей и реле, некоторых видов компактных люминесцентных ламп (КЛЛ), люминесцентных ламп с холодным катодом или с внешним электродом, ртутных термометров и приборов измерения давления. Конвенция вводит регулирование использования ртути и ограничивает ряд промышленных процессов и отраслей, в том числе горнодобывающую (особенно непромышленную добычу золота), производство цемента.
Способ экспрессного контроля ртути в почвах и биологических объектах предусматривает разложение исследуемого материала смеси хлoристoводородной и азотной кислот при воздействии ультразвуком и определение содержания ртути в этом растворе посредством ртутного анализатора. Разложение исследуемого материала осуществляют в одну стадию. Ультразвуком воздействуют в течение 4-6 мин во время этой стадии разложения материала. Способ позволяет упростить технику анализа за счет выполнения ультразвукового разложения проб в одну стадию и увеличить экспрессность определения рути в биологических объектах.
Изобретение относится к области аналитической химии, а именно к методам определения ртути в экологических объектах, и может быть использовано для экспрессного контроля ртути в биологических материалах растительного происхождения, в т.ч. пищевых продуктах.
Среди ряда актуальных проблем мониторинга природных объектов немаловажное значение имеют вопросы контроля технологического загрязнения токсичными материалами, в т.ч. ртути. Биологические объекты растительного происхождения, в т. ч. пищевые продукты — важное звено в экологической цепи, которое является наряду с водой, источником поступления ртути в организм человека и животных.
3. Применение ионоселективных электродов
В связи с интенсивным загрязнением почв различными вредными веществами и их накоплением в почве происходит постепенному изменение физико-химических свойств почвы, что в дальнейшем сокращается численность почвенной мезофауны, и снижается плодородие почвы. Поэтому чрезвычайно важно изучение ее современного состояния и изменения под влиянием антропогенной деятельности.
Ионометрия является очень специфичным методом анализа. От других методов анализа ионометрию выгодно отличает то, что во многих случаях для определения концентрации раствора его не требуется отделять от твердой фазы. Это позволяет исключить из процесса анализа такую трудоемкую операцию, как фильтрование или центрифугирование. Примером может служить хорошо известное измерение рН с помощью стеклянного ионоселективного электрода. Важным достоинством является также то, что для ионометрических измерений выпускаются малогабаритные, вплоть до карманных, переносные приборы на батарейном питании, что позволяет использовать их в полевых условиях.
Другой особенностью метода является то, что он измеряет не общую концентрацию химического элемента в растворе, а только свободного иона, в виде которого находится элемент в растворе и к которому чувствителен данный электрод. Эта особенность ионометрии несколько осложняет ее использование для определения общих концентраций веществ в растворах и требует применения специальных приемов, позволяющих получать результаты близкие тому, что дают общепринятые методы количественного анализа.
Как отмечено выше, ЦИНАО разработаны и стандартизованы методики рН-метрического определения гидролитической кислотности почв и хлорида в водной вытяжке из засоленных почв. Для анализа грунтовых и поливных вод использование ионоселективных электродов предложено для определения хлорида, кальция, нитратов, фторидов.
Широкое применение получило ионометрическое определение нитратов. Было разработано определение нитратов в почвах, водах, кормах и растениях, в тепличных грунтах. Широкое применение метод нашел при анализе продукции растениеводства. Методика, разработанная ЦИНАО и апробированная Институтом питания РАМН, была утверждена Госагропромом СССР и Минздравом СССР.
Благодаря простоте и экспрессности эта методика в настоящее время повсеместно используется для токсикологического контроля. Определение нитратов с помощью нитратного электрода стандартизовано для анализа почв ГОСТ 26951.
Для определения аммонийного азота разработаны методики анализа с использованием аммиачного газочувствительного электрода. Метод применен для анализа почв, что в сочетании с ионометрическим определением нитратов обеспечивает экспрессное определение запасов минерального азота в почвах, а также могут быть использованы для определения азотминерализующей способности почв: нитрификационной способности.
Разработаны методики определения калия в тепличных грунтах с помощью ионоселективного электрода, нитритов в кормах и растениях ионометрическим методом, фтора в вытяжках из почв, в продукции растениеводства и кормах, аммиачного азота в кормах и растениях, легкоподвижного калия в почвах.
Источник: ecomonitoring2020.blogspot.com
Новая процедура определения золота в рудах, почвах и отходах методом электротермического атомно-абсорбционного анализа

Декабрь, 2021 – Санкт-Петербург, Россия. Простота и безопасность электротермического варианта атомно-абсорбционного анализа в сочетании с высокой чувствительностью и селективностью спектрометров МГА-1000 выводят определение драгоценного металла на новый уровень удобства.
Большинство рутинных методик атомно-абсорбционного (АА) определения золота в рудах, золотосодержащих отходах и аналогичных объектах предполагает кислотное разложение проб с последующим концентрированием определяемого элемента на твердом сорбенте либо путем его экстрагирования в органический растворитель. Это усложняет саму процедуру анализа, требует использования дополнительных реагентов и расходных материалов, создает проблему утилизации органических растворителей. Организация рабочего места в случае применения пламенного варианта АА-анализа дополнительно усложняется из-за необходимости монтажа линий подачи горючего газа и связанных с этим финансовых и административных препятствий.
ГК «Люмэкс» предложила новую упрощенную процедуру, исключающую предварительное концентрирование золота при определении его содержания в пробе свыше 1 г/т (мг/кг). После кислотного разложения солянокислый раствор пробы вносят непосредственно в графитовую печь спектрометра МГА-1000 и проводят измерение. При необходимости определения золота в диапазоне от 0,02 до 1 г/т элемент предварительно экстрагируют из солянокислых растворов изоамиловым спиртом, который малотоксичен и не требует специальных условий утилизации.
При процедуре не используются дорогие или специализированные реактивы, а также дополнительные расходные материалы и приставки к АА спектрометру.
Источник: www.lumex.ru
Определение золота в почвах
Эвкалипт, акация (листья)
Сцинтилляционным эмиссионным спектральным анализом (с.э.с) было показано, что большинство золота в золе растений, отобранных над золоторудными месторождениями, находится в растениях в свободном состоянии [3]. Однако золото, находящееся в растениях в коллоидном состоянии, с.э.с.-анализом не регистрируется. Золото в ионной или коллоидной формах перемещается в почвах за счет циркуляции воды и в результате абсорбции усваивается корнями растений [4]. Было установлено, что скорость перемещения золота в растениях прямо пропорциональна скорости испарения влаги с их поверхности. При этом наибольшая скорость передвижения золота и его концентрация растениями наблюдается весной.
Шлемник байкальский – многолетнее травянистое лекарственное растение. Имеет монголо-даурско-маньчжурский тип ареала. В России встречается в Восточном Забайкалье, Среднем Приамурье, юго-западном Приморье. Основными действующими веществами растения являются флавоноиды.
Настойки из корней шлемника издавна применяются в тибетской, китайской, дальневосточной народной и официальной медицине как гипотензивное, седативное средство, а также как антимутагенное, ингибирующее образование метастазов средство при лечении онкологических заболеваний [2, 7]. Установлено влияние ряда микроэлементов (алюминия, бария, кобальта, хрома, меди, железа, марганца, молибдена) на накопление флавоноидов в шлемнике байкальском [5]. Определено также, что надземная часть шлемника байкальского является умеренным накопителем алюминия, бария, хрома, меди, железа, марганца, реже ванадия, причем для железа и марганца наблюдаются случаи сверхконцентрирования.
Материалы и методы исследования
Материал отбирался из естественных мест произрастания: Приморский край (Чернятино, Пограничный, Комиссарово), Амурская область (Семеновка, Свободный, Благовещенск), Читинская область: Карымский район (Ключи, Бишигино, Матусово, Карымское), Борзинский и Приаргунский районы (Борзя, Ключевское, Тасуркой, Октябрьское), а также интродуцированный в Центральном сибирском ботаническом саду СО РАН (г. Новосибирск). Сбор материала производился во время цветения и после созревания семян. Отбор образцов растений и почвы производился вне рудных месторождений и вдали от населенных пунктов, в местах, незагрязненных техногенными отходами.
Образцы растений промывались дистиллированной водой, высушивались при 80 °С в течение двух суток, после чего истирались в агатовой ступке. Озоление материала не проводилось, т.к. при этом образуются комплексные легко летучие соединения золота с углеродом, что приводит к занижению результатов анализов. Определение золота (85 анализов) из почвы и различных частей растения производилось нейтронно-активационным методом в НИИ ЯФ при Томском политехническом университете (аналитик В.И. Резчиков) из навески 50 г воздушно-сухого сырья. Чувствительность НАА n•10–9 мас. %.
Результаты исследования и их обсуждение
Исследование уровней накопления золота в почвах и в разных частях шлемника из естественных мест произрастания и при интродукции показало, что золото в тех или иных количествах установлено во всех проанализированных пробах.
По уровням накопления золота в разных частях шлемника (корнях, стеблях, листьях, семенах, чашечках) можно отметить некоторые закономерности. Для растений из Приморского края, Амурской области, Борзя-Приаргунского района Читинской области наблюдается тенденция к несколько большему накоплению золота в корнях и коре корня. Для растений из Карымского района Читинской области содержания золота в коре корня и цветках близки. Содержание золота в шлемнике, интродуцированном в ЦСБС, в 2–3 раза выше в чашечках и цветках, чем в других частях растений. Не всегда большие содержания золота в почвах дают повышенные концентрации его в растении.
Для характеристики отношения содержания какого-либо элемента в организме к содержанию его в окружающей среде определяют коэффициент биологического накопления (КБН). В естественных местах произрастания шлемника КБН золота для разных частей растения много меньше единицы.
Для Приморского края, Амурской области и Борзя-Приаргунского района самый низкий КБН отмечен для верхних частей стебля в пределах от (0,13; 0,44; 0,02 соответственно). Для корня КБН золота для этих местообитаний несколько выше (0,26; 0,27; 0,10 соответственно). Для коры корня растений Борзя-Приаргунского района КБН составил 0,24.
Для растений из популяций шлемника Карымского района КБН на порядок ниже: 0,005 для верхней части стебля и не превышает 0,07 для остальных частей растения, кроме цветков, где он повышается до 0,38. И только для надземной части растений из ЦСБС КБН близок к единице и даже превышает её: нижняя часть стебля – 0,73, цветки – 0,92, чашечки – 1,19). Для остальных частей интродуцированных растений КБН золота изменяется в пределах от 0,09 для средней части стебля до 0,37 для верхней части стебля. КБН для корней растений из ЦСБС – 0,13, для коры корня – 0,33.
Низкие концентрации золота в шлемнике, возможно, свидетельствуют о том, что растение обладает антиконцентрационным барьером, не допускающим накопление элемента выше токсичных для данного растения концентраций [1, 3]. Также установлено, что кальций выполняет роль элемента-антагониста по отношению к золоту и другим элементам [8]. Аномальные концентрации кальция в почвенных водах уменьшают миграцию золота, что влияет на его накопление растениями.
Содержание золота в корнях шлемника изменяется в пределах 1,3 до 11,4 мг/т, и оно для природных местообитаний чаще несколько выше, чем для других частей растения (рисунок).
Нужно отметить, что исследованные особи шлемника из естественных мест произрастания имели возраст более 20 лет, растения, интродуцированные в ЦСБС, были более молодыми (возраст до 7 лет).
Корни шлемника из разных мест произрастания имеют близкие средние содержания золота – 3,5–8,1 мг/т. В молодых корнях интродуцированных в ЦСБС растениях концентрация золота в 2–3 раза ниже, чем в старых корнях растений природных местообитаний. Установлено, что золото накапливается в коре корня в 2–3 раза больше, чем в остальной части корня, средние содержания – 6,2–12,8 мг/т. При этом уровень накопления золота в корнях шлемника имеет, вероятно, определенный предел и не зависит от содержания его в почвах.
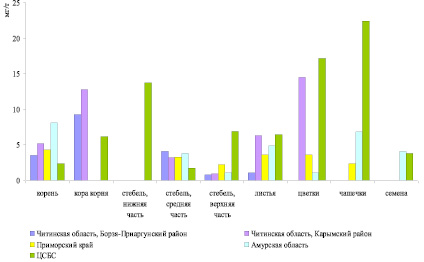
Содержание золота (мг/т) в шлемнике байкальском из разных мест произрастания
Содержание золота в цветках шлемника из разных мест произрастания изменяется в широких пределах от 3,6 до 17,2 мг/т. Наиболее высокие концентрации золота в цветках растений из п. Матусово Карымского района Читинской области (14,5 мг/т) и интродуцированного в ЦСБС (17,2 мг/т).
Таким образом, проведенное исследование показало, что золото в шлемнике байкальском (Scutellaria baicalensis Georgi, Lamiaceae) накапливается во всех частях растения. Его концентрация в растении не всегда зависит от уровня его содержания в почве.
Низкие концентрации золота в шлемнике, возможно, свидетельствуют о том, что растение обладает антиконцентрационным барьером, не допускающим накопление элемента выше токсичных для данного вида концентраций.
Не было выявлено общей закономерности в накоплении золота по разным частям растения. Наблюдается только тенденция к уменьшению содержания золота от корней к стеблям, листьям, семенам, чашечкам для шлемника из естественных мест произрастания (возраст растений свыше 20 лет). А для шлемника, интродуцированного в ЦСБС (возраст растений до 7 лет), накопление золота происходит в наземной части растения, особенно в цветках и чашечках. КБН для природных местообитаний ниже единицы. У молодых интродуцированных растений из ЦСБС КБН близок к единице и даже превышает ёе (цветки, чашечки).
При использовании растений в качестве лекарственных средств необходимо учитывать их микроэлементный состав. Дальнейшее изучение влияния микроэлементов, в том числе золота, на организм человека и интерпретация полученных данных требует всестороннего анализа и комплексного подхода.
Сведения об элементном составе, в том числе о золоте, шлемника байкальского могут использоваться в геологии при поиске месторождений полезных ископаемых биогеохимическим методом.
Работа выполнена при финансовой поддержке Государственного задания «Наука» № 3805.
Источник: natural-sciences.ru