Анодная медь является сложным многокомпонентным сплавом. Обычно она содержит, %: 99,5-99,8 меди, до 0,015 серы, столько же железа, до 0,5 никеля, до 0,05 свинца, до 0,01 висмута, до 0,2 мышьяка, до 0,06 селена+теллура, до 0,03(300г/т) золота и до 0,5(5000 г/т) серебра. Электролитическое рафинирование меди преследует две цели:
1) Получение меди высокой чистоты (99,90-99,99% меди)
2) Извлечение попутно с рафинированием благородных металлов и других ценных компонентов (селен, теллур, никель, висмут и др.)
Электролитическое рафинирование меди основано на различии ее электрохимических свойств и содержащихся в ней примесей. Медь – это электроположительный металл, ее нормальный потенциал +0,34В.
Для осуществления электролитического рафинирования меди аноды, отлитые после огневого рафинирования, помещают в электролизные ванны, заполненные сернокислым электролитом
Между анодами в ваннах располагаются тонкие медные листы – катодные основы. При включении ванн в сеть постоянного тока происходит электрохимическое растворение меди на аноде, перенос катионов через электролит и осаждение ее на катоде.
Рафинирование серебра
Примеси меди при этом в основном распределяются между шламом(твердым осадком на дне ванн) и электролитом. В результате электролитического рафинирования получают:
— Шлам, содержащий благородные металлы, селен, теллур
— Загрязненный электролит, часть которого используют для получения медного и никелевого купороса.
Кроме того, вследствие неполного электрохимического растворения анодов, получают анодные остатки (анодный скрап).
Анодный процесс: Cu — 2e = Cu 2+
Катодный процесс: Cu 2+ + 2e = Cu
Электроположительный потенциал меди позволяет выделить медь на катоде из кислых растворов без опасения выделения водорода. Введение в электролит наряду с медным купоросом свободной серной кислоты существенно повышает электропроводность раствора.
Промышленные электролиты обычно содержат 30-50 г/л Cu 2+ и 120-170 г/л свободной серной кислоты. Для улучшения качества катодной поверхности, в электролиты вводят разнообразные поверхностноактивные (коллоидные) добавки – клей (чаще столярный), желатин, сульфидный щелок, тиомочевину и так далее. Добавки непрерывно вводят в циркулирующий электролит, обычно применяя одновременно две добавки. На одну тонну катодной меди расходуют 15-40 г клея, 15-20 г желатина, 20-60 г сульфидных щелоков или 60-100 г тиомочевины.
Температура электролита составляет 55-65С. Основными требованиями, предъявляемыми к электролиту, является его высокая электропроводность и чистота, однако реальные электролиты, помимо сульфата меди, серной кислоты, воды и необходимых добавок обязательно содержат растворенные примеси, содержавшиеся до этого в анодной меди.
Примеси, более электроотрицательные чем медь (никель, железо, цинк и др.) практически полностью переходят в электролит. Исключение составляет только никель, около 5% которого осаждается в шлам. Более электроположительные по сравнению с медью примеси (благородные металлы) переходят в шлам. Золото на 99,5% от его содержания в анодах, а серебро – на 98.
Электролитическое рафинирование меди
Основными характеристиками, определяющими параметры и показатели электролиза меди являются:
— Выход металла по току
— Напряжение на ванне
— Удельный расход электроэнергии.
Плотность тока выражается в амперах на единицу поверхности электрода (D=I/S). Единицы измерения – А/м 2 катода.
По закону Фарадея, на каждый А*ч электричества осаждается 1 электрохимический эквивалент металла. Для меди он равен 1,1857 г/А*ч. Следовательно, с увеличением плотности тока производительность процесса электролиза растет. Чаще всего заводы работают при плотности тока 240-300 А/м 2 , но можно довести плотность тока до 500 А/м 2 .
Степень использования тока на основной электрохимический процесс называется выходом металла по току. Выход по току может быть выражен в долях единиц или в процентах. На величину потерь тока влияют: утечки тока, возникающие в результате заземления в цепи, утечки тока через циркуляционные трубопроводы электролита, короткие замыкания между электродами, побочные химические и электрические процессы, нагревание электролита и контактов.
С этой целью введено понятие коэффициента использования тока или, как принято в заводской практике, “выход по току”, который рассчитывается как отношение фактически полученного количества меди к теоретически возможному при данных условиях электролиза (сила тока, продолжительность электролиза)
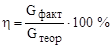
Напряжение на ванне составляет от 0,35 до 0,46 В.
Удельный расход электроэнергии – 280-370кВт*час/тонну меди
В настоящее время для электролиза меди в основном используются цельнолитые железобетонные ванны ящичного типа. Внутри электролизные ванны облицовывают винипластом. Ванны установлены на столбах с изоляторами из стекла, фарфора или текстолита на высоте 4-5м от 0 отметки. Под ваннами расположены насосы, трубопроводы и сборники электролита.
Для спуска шлама и раствора в днищах имеется отверстие с пробкой. Если стоков не делают, ванны разгружают с помощью насосов.
Электролизные ванны объединяют в блоки по 5-20 штук, а блоки – в серии. В электрическую схему питания постоянным током ванны в блоках и блоки в сериях включены последовательно, а электроды в отдельных ваннах – параллельно. Эта система включения ванн и электродов получила название мультипль. Аноды отливают с ушками, которыми они опираются на токоподводящие шины и борта ванн.
Средняя толщина анода 35-45 мм, масса – до 350кг. Для обеспечения равномерного растворения анодов по высоте электролита, их отливают клиновидной формы с утолщением кверху. Катодные основы изготавливают из медных листов, размер катодной основы превышает размер анода по длине на 25-50 мм, по ширине на 50-60 мм. Катодные основы подвешивают в ваннах на медных трубчатых штангах.
Расстояние от боковых кромок катодов до стенок ванн около 300 мм, до днища ванны 400-600 мм, число анодов, завешиваемых в одну ванну, на разных заводах колеблется от 29 до 48 штук. Число катодов в ванне всегда на 1 больше числа анодов, что обеспечивает равномерное растворение всех анодов, включая крайние. Расстояние между осями одноименных электродов – около 110мм, соответственно, между анодом и катодом – примерно 35-40 мм.
Электролит обычно подают в нижнюю зону ванны, а отводят сверху. В зависимости от применяемой плотности тока и массы анодов, каждую партию катодов наращивают в течение 6-10 суток. За это время катоды достигают толщины 8-10 мм. Срок срабатывания анодов соответствует 2-3 заменам катодов и достигает 30 суток. Загрузку в ванны анодов осуществляют мостовым краном.
Извлеченные из ванн катоды направляют на промывку от электролита, загрязняющего их серой. Промывку ведут последовательно оборотными растворами и чистой горячей водой. Отмытые катоды переплавляют с получением слитков для волочения проволоки (вайербарсы) или медной катанки. Отработанные аноды(анодные остатки) переплавляют в анодных печах.
Выгрузку анодного шлама и полный слив электролита осуществляют периодически после полного срабатывания нескольких партий анодов(в зависимости от выхода шлама). Для выпуска шлама две соседние ванны выключают(шунтируют) наложением специальных медных шунт. После этого, из ванны извлекают электроды, сливают электролит и на дне остается слой сгущенного шлама.
Его сливают и смывают в специальные емкости. После разгрузки ванны ее зачищают от обвалившихся кусочков меди, уплотнившегося шлама, и промывают. Шлам пропускают через рокот для отделения крупной фракции меди, после чего фильтруют и направляют на специальную переработку.
Технико-экономические показатели процесса:
1) Содержание меди в анодах, % 99-99,8
2) Масса анодов, кг 175-350
3) Время растворения анодов, сутки 18-27
4) Выход анодных остатков, % 17-20
5) Время наращивания катодов, сутки 6-9
6) Масса катода, кг 70-140
7) Выход шлама, % 0,8 – 8,5
8) Состав электролита, г/л Cu 2+ 50, H2SO4 125-230, коллоидные добавки 30-300
9) Температура электролита, С 55-65
10) Скорость циркуляции, л/мин 6-15
11) Катодная плотность тока А/м 2 180-300
12) Напряжение на ванне, В 0,25-0,4
13) Расход электроэнергии кВт*ч/т кат меди 230-350
Понравилась статья? Добавь ее в закладку (CTRL+D) и не забудь поделиться с друзьями:
Источник: studopedia.ru
3.3.5. Рафинирование меди
Черновая медь всегда подвергается рафинированию для удаления из нее примесей, ухудшающих ее свойства, а также для извлечения из нее золота и серебра. В современной практике рафинирование проводят последовательно двумя принципиально различными методами: пирометаллургическим и электролитическим.
Огневое (пирометаллургическое) рафинирование меди проводят в отражательных печах. В отличие от отражательных печей для получения штейна эти печи меньших размеров (ширина 5 м, длина 12 — 15 м, глубина ванны 0,9 м).
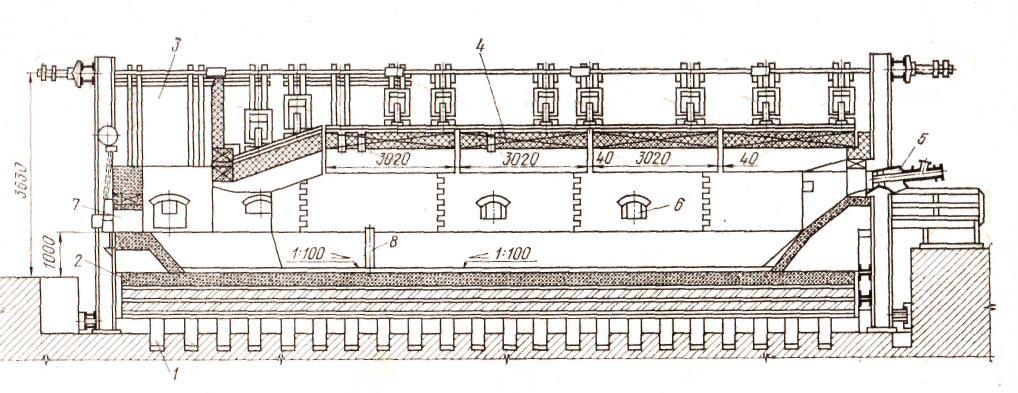
Рис.10. Отражательная печь для рафинирования меди:
1 – столбчатый фундамент; 2 – подина; 3 – газоход; 4 –распорно-подвесной свод; 5 – горелка; 6 – рабочее окно с заслонкой; 7 – шлаковое окно; 8 – щелевая летка
Весь цикл огневого рафинирования состоит из операций: загрузки и расплавления, окисления примесей, удаления газов, раскисления меди и разливки; он занимает обычно 12 — 16 ч. Примеси в черновой меди окисляют воздухом, который вдувают через стальную трубку диаметром 20 — 40 мм, футерованную огнеупорами и погружаемую в расплавленную медь.
Медь после огневого рафинирования подают на разливочные машины для отливки анодов, квадратных плит с ушками, имеющими толщину 40 — 50 мм, длину и ширину — ~ 1 м . Указанные аноды направляют на электролитическое рафинирование. Анодная медь содержит 99,4 – 99,6 % меди, остальное примеси, в том числе золото, серебро, селен и теллур. В среднем в 1 т меди содержится 30 – 100 г золота и до 1000 г серебра. Такую медь обязательно подвергают рафинированию методом электролиза.
3.3.5.2. Электролитическое рафинирование меди
Анодная медь содержит 99,4 — 99,6 % Сu; остальное приходится на долю оставшихся после огневого рафинирования примесей, включая золото, серебро, селен и теллур. В среднем в 1 т анодной меди содержится 30 — 100 г золота и до 1000 г серебра.
Одним из методов очистки от примесей является электролитическое рафинирование, основанное на различии потенциалов выделения из растворов различных элементов.
Следовательно электролитическая ячейка состоит из катода, анода и электролита, рис. 11.
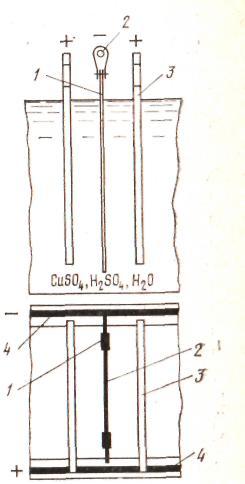
Рис. 11. Схема электролитического рафинирования меди: 1- катод; 2 – катодная штанга; 3 – анод; 4 – токоподводящие шины
Электролит – водный раствор сульфата меди (160 – 200 г/л) и серной кислоты (135 – 200 г/ л). Анод – литая черновая медь; катод – матрица – тонкие лист из электролитной меди
В черновой меди элементы подразделяются на элементы имеющие различный потенциал выделения по отношению к водороду:
- Электроотрицательные – Fe, Ni, Co, Zn, Sn, Pb, которые практически полностью растворяются на аноде, могут попасть в раствор и выделиться на катоде совместно с медью, если их концентрация становится выше определенного предела. Для избежания их выделения необходимо не допускать повышение их концентрации выше определенного предела или предварительно от них очищаться другими методами ;
- Близкие потенциалы выделения к меди – As, Sb, Bi. Их переход в катодный металл наиболее вероятен. Для избежания их выделения электролит периодически выводится из цикла и подвергается регенерации;
- Электроположительные — Au, Ag. В условиях электролиза не растворяются и остаются в анодном шламе.
- Примеси химических соединений — Cu2S, Cu2Se, Cu2Te. Вследствие электрохимической нейтральности и малой растворимости в электролите переходят в шлам совместно с благородными металлами.
Механизм электролитического рафинирования меди включает следующие элементарные стадии:
- электрохимическое растворение меди на аноде с отрывом электронов и образованием катиона:
Сu -2 е → Сu 2+ ;
- перенос катиона через слой электролита к поверхности катода;
- электрохимическое восстановление катиона меди на катоде:
Cu 2 + 2 e → Cu; 4) внедрение образовавшегося атома меди в кристаллическую решетку катода (рост катодного осадка). Электролитическое рафинирование меди проводят в ваннах, наполненных раствором сернокислой меди, подкисленным серной кислотой. Размеры ванн зависят от размеров и числа электродов. В ваннах устанавливают до 45 катодов и 44 анода. Корпуса ванн изготовляют из бетона или дерева, стенки ванны внутри покрывают винипластом, свинцом или другим кислотоупорным материалом. Аноды соединяют с положительным полюсом источника постоянного тока (рис. 12). Ионы меди из раствора восстанавливаются и плотными кристаллами оседают на катодных основах. 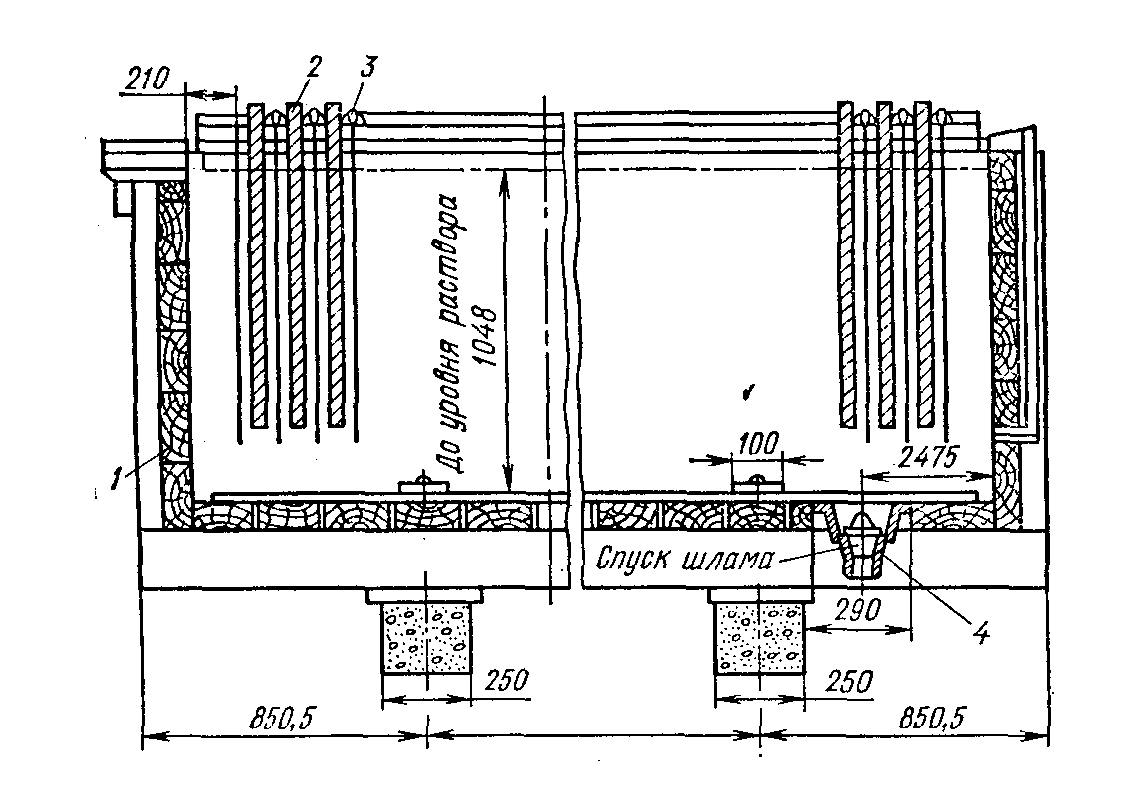
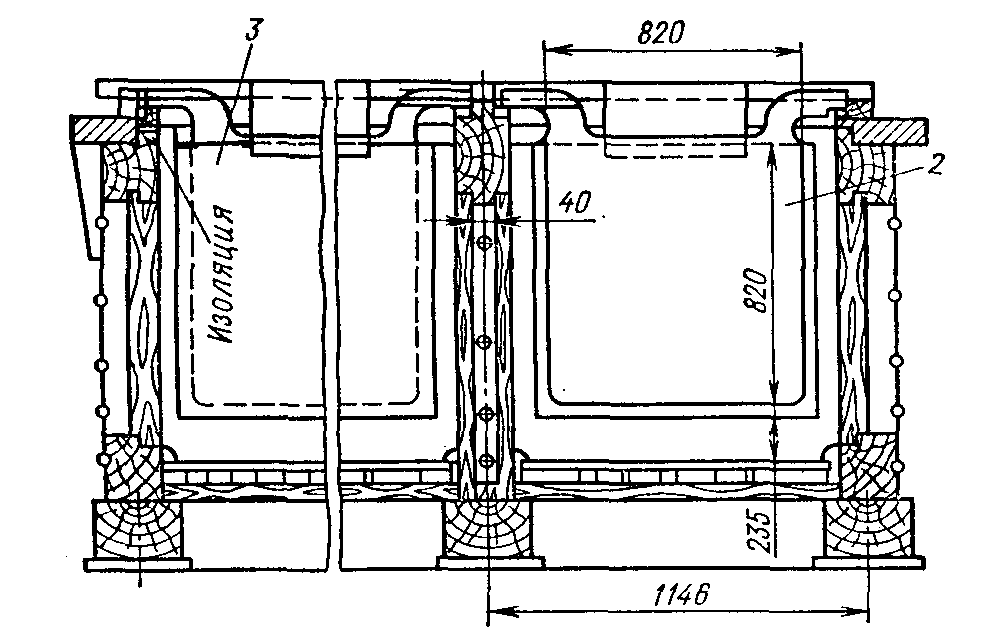 Рис. 12. Электролизная ванна для рафинирования меди: 1 — деревянный корпус ванны; 2 — аноды; 3 — катоды; 4 — отверстие для удаления шлака Катоды, извлеченные из ванн, тщательно промывают водой, а затем их направляют для переплавки или производства сплавов в электрических или отражательных печах.
Рис. 12. Электролизная ванна для рафинирования меди: 1 — деревянный корпус ванны; 2 — аноды; 3 — катоды; 4 — отверстие для удаления шлака Катоды, извлеченные из ванн, тщательно промывают водой, а затем их направляют для переплавки или производства сплавов в электрических или отражательных печах.  Сульфатная медь
Сульфатная медь  В электролизном цехе (электролитическая ванна)
В электролизном цехе (электролитическая ванна)
Источник: studfile.net
Электролитическое рафинирование меди

Рафинирование – заключительный этап в цепочке получения из медной руды «чистого» металла. Он состоит из двух последовательных этапов – пирометаллургическое и электролитическое рафинирование. В первом черновая медь (содержит до 4% примесей) обрабатывается в печах и из неё удаляются все примеси, кроме включений серебра, золота, селена и теллура, при этом чистота основного металла может достичь 99,6%. Во втором с помощью электролитических ванн получают полностью очищенную медь, доля примесей в которой не превышает 0,001%.
Рассмотрим подробнее процесс электролитического рафинирования. Речь идёт исключительно о промышленном производстве, в работе чаще всего используются гальванические ванны объемом 4-12 м 3 метра, в качестве электролита выступает смесь из сернокислой меди (CuSO4), подкисленной серной кислотой (H2SO4).
В смесь погружаются аноды из меди, прошедшей пирометаллургическое рафинирование, и катоды из «чистой» меди. В ходе электролиза все примеси остаются в растворе электролита, а на катоде оседает очищенный металл. После завершения процесса катод, по сути, представляет собой готовый слиток меди, который можно как отправить предприятиям-потребителям напрямую, так и переплавить в слитки или иной требуемый тип проката. Часть «вымытых» из меди примесей оседает на дно ванны (т.н. шлам), в дальнейшем их можно подвергнуть последующей переработке с целью получения ценных металлов.
Промышленный процесс электролитического рафинирования предполагает работу с большими объёмами металлов, электролитов и, как следствие, высокие сопутствующие затраты (стоимость электролитов, электричество, потери и т.д.). В ходе рафинирования анод («загрязнённая» медь) постепенно растворяется, теряя в объёме – часть примесей оседает на дно ванны, часть растворяется в электролите. При этом «чистая» медь «нарастает» на катоде, постепенно увеличивая его в размерах. Начальная фаза изображена на рисунке ниже.

В рафинировании меди применяется такое понятие как экономическая плотность тока – плотность тока, при которой затраты электроэнергии на получение 1 тонны чистой меди будут минимальными (не путать с таковой при расчете сечения проводов, когда идет расчет электрических потерь в ЛЭП). При этом время процесса зачастую бывает не оптимальным или вовсе не принимается во внимание из-за решающей роли стоимости электричества. Так, в среднем на растворение анода требуется 20-30 суток, а катоды достигают оптимального размера за 6-12 суток при стандартной плотности тока 170-200 А/м 2 и напряжении между анодом и катодом 0,3-0,4 В. Расход электроэнергии при этом составляет в среднем 230-350 кВт*ч на 1 тонну меди.
Тем не менее, время тоже является важным фактором, напрямую влияющим как на себестоимость процесса получения медного проката, так и на общую производительность предприятия. Уменьшить время процесса рафинирования можно одним способом – увеличением плотности тока до более высоких, по сравнению со стандартными, значений. При этом, разумеется, придётся изменять многие параметры процесса, чтобы использование токов высокой плотности оставалось в рамках «экономической плотности». Для выполнения этого условия в ход идут различные методики, дополняющие друг друга:
1) Поиск сочетаний поверхностно-активных веществ (ПАВ), которые улучшают свойства электролита,
2) Использование различных схем циркуляции электролита, позволяющих повысить скорость до 20 л/мин на 1 см 2 поверхности (при этом плотность тока может достигать 860 А/м 2 ),
3) Применение реверсного тока в процессе рафинирования. Оптимальным на данный момент является соотношение прямого и реверсного тока 200:10. Этот метод является в настоящее время самым эффективным, но требует надёжного источника питания, позволяющего генерировать импульсы тока, строго соответствующие заданным параметрам.
Все описанные выше средства в настоящее время активно исследуются и совершенствуются на многих металлургических предприятиях в России и за рубежом. Основной их целью является не только ускорение процесса, но и обеспечение его непрерывности и повышение эффективности, в том числе экономической.
Первые два способа, как правило, обкатываются непосредственно на предприятиях в ходе экспериментов – проверяются новые комбинации ПАВ, меняется состав электролита, строятся новые системы подачи электролита для повышения скорости его циркуляции. Использование же реверсных токов зачастую становится самым доступным методом – для его внедрения в промышленный процесс достаточно изменить схему питания гальванической ванны, применив современный источник тока и обеспечив циркуляцию электролита.
Хорошим решением этой задачи будет использование источников питания российского предприятия «Навиком», разрабатывающего источники питания для промышленного применения.
Источник: navicom.org