В данную товарную позицию включаются драгоценные металлы, указанные в группе 71 (то есть серебро, золото, платина, иридий, осмий, палладий, родий и рутений), при условии, что они находятся в коллоидном состоянии. Эти драгоценные металлы в коллоидном состоянии получают путем диспергирования или катодного распыления, или восстановлением одной из их неорганических солей.
Коллоидное серебро находится в виде небольших зерен или хлопьев голубоватого, коричневатого или зеленовато–серого цвета с металлическим блеском. Оно используется в медицине как антисептик.
Коллоидное золото может быть красным, фиолетовым, голубым или зеленым и используется для тех же целей, что и коллоидное серебро.
Коллоидная платина находится в виде мелких серых частиц и обладает замечательными каталитическими свойствами.
Эти металлы в коллоидном состоянии (например, золото) включаются в данную товарную позицию, если они поставляются в виде коллоидного раствора, содержащего защитные коллоиды (такие как желатин, казеин, рыбий клей).
Неорганическая химия. Металлы: Медь, серебро, золото. Лекция 8
(Б) НЕОРГАНИЧЕСКИЕ ИЛИ ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
ДРАГОЦЕННЫХ МЕТАЛЛОВ, ОПРЕДЕЛЕННОГО
ИЛИ НЕОПРЕДЕЛЕННОГО ХИМИЧЕСКОГО СОСТАВА
Это следующие соединения:
(I) Оксиды, пероксиды и гидроксиды драгоценных металлов, аналогичные соединениям подгруппы IV.
(II) Неорганические соли драгоценных металлов, аналогичные соединениям подгруппы V.
(III) Фосфиды, карбиды, гидриды, нитриды, силициды и бориды, аналогичные соединениям товарных позиций 2849, 2850 и 2853 (такие, как фосфид платины, гидрид палладия, нитрид серебра, силицид платины).
(IV) Органические соединения драгоценных металлов, аналогичные соединениям группы 29.
В данную товарную позицию включаются также соединения, содержащие как драгоценные металлы, так и другие металлы (например, двойные соли недрагоценного металла и драгоценного металла, сложные эфиры, содержащие драгоценные металлы).
Наиболее распространенные соединения драгоценных металлов перечислены ниже:
(1) Соединения серебра:
(а) оксиды серебра. Оксид дисеребра (Ag2O) представляет собой коричневато–черный порошок, малорастворимый в воде. На свету он становится черным.
Оксид серебра (AgO) – серовато–черный порошок.
Оксиды серебра используются, inter alia, в производстве аккумуляторов;
(б) галогениды серебра. Хлорид серебра (AgCl) – белая масса или плотный порошок, не растворимый в воде, темнеющий на свету; его упаковывают в темноокрашенные непрозрачные контейнеры. Используется в фотографии, в производстве керамики, в медицине и для серебрения.
Кераргириты (или роговая серебряная обманка), природные хлориды и йодиды серебра не включаются (товарная позиция 2616).
Бромид серебра (желтоватый), йодид серебра (желтый) и фторид серебра используются для тех же целей, что и хлориды;
(в) сульфид серебра. Искусственный сульфид серебра (Ag2S) – тяжелый серо–черный порошок, не растворимый в воде, используется для получения стекла.
Природный сульфид серебра (аргентит), природный сульфид серебра и сурьмы (пираргирит, стефанит, полибазит) и природный сульфид серебра и мышьяка (прустит) не включаются (товарная позиция 2616);
Добыча золота БУДУЩЕГО! Как связаны между собой ЗОЛОТОДОБЫЧА и ХИМИЯ?! | Наука Просто
(г) нитрат серебра (AgNO3) – белые кристаллы, растворимые в воде, токсичные, повреждают кожу. Используется для серебрения стекла или металлов; для окрашивания шелка или рога; в фотографии; для производства несмываемых чернил; как антисептик или средство против паразитов. Иногда его называют «ляпис», хотя это название также применимо к нитрату серебра, сплавленному с небольшим количеством нитрата натрия или калия, а иногда и с небольшим количеством хлорида серебра, с целью получения прижигающих средств (группа 30);
(д) прочие соли и неорганические соединения.
Сульфат серебра (Ag2SO4), кристаллы.
Фосфат серебра (Ag3PO4), желтоватые кристаллы, малорастворимые в воде; используются в медицине, фотографии и оптике.
Цианид серебра (AgCN), белый порошок, темнеющий на свету, не растворимый в воде; используется в медицине и для электроосаждения серебра. Тиоцианат серебра (AgSCN) имеет аналогичный вид и используется как усилитель в фотографии.
Комплексные цианидные соли серебра и калия (KAg(CN)2) или серебра и натрия (NaAg(CN)2) представляют собой белые растворимые соли, используемые при нанесении электролитического покрытия.
Фульминат серебра (гремучее серебро), белые кристаллы, взрывающиеся при легком ударе, опасные в обработке; используются для производства капсюлей–детонаторов.
Дихромат серебра (Ag2Cr2O7), кристаллический рубиново–красный порошок, малорастворимый в воде; используется при исполнении художественных миниатюр (серебряный красный, пурпурный красный).
Перманганат серебра, кристаллический темно–фиолетовый порошок, растворимый в воде; используется в противогазах.
Азид серебра, взрывчатое вещество;
(е) органические соединения серебра. Они включают:
(i) лактат серебра (белый порошок) и цитрат серебра (желтоватый порошок); используются в фотографии и как антисептики;
(ii) оксалат серебра, который разлагается и взрывается при нагревании;
(iii) ацетат, бензоат, бутират, циннамат, пикрат, салицилат, тартрат и валерат серебра;
(iv) протеинаты, нуклеаты, нуклеинаты, альбуминаты, пептонаты, вителлинаты и таннаты серебра.
(2) Соединения золота:
(а) оксиды. Оксид одновалентного золота (Au2O). Нерастворимый темно–фиолетовый порошок. Оксид трехвалентного золота (Au2O3) (ангидрид трехвалентного золота) – коричневый порошок; соответствующая кислота – гидроксид золота или кислота (Au(OH)3), черный продукт, разлагающийся на свету, из которого получают аураты щелочных металлов;
(б) хлориды. Хлорид одновалентного золота (AuCl), желтоватый или красноватый кристаллический порошок. Трихлорид золота (AuCl3) (хлорид трехвалентного золота, бурый хлорид) – красновато–коричневый порошок или кристаллическая масса, очень гигроскопичная, часто поставляется в герметичных канистрах или тубах. Тетрахлорзолотая (III) кислота (AuCl3·HCl·4H2O) (желтый хлорид) – желтые кристаллы, гидратированные, и хлораураты щелочных металлов – красновато–желтые кристаллы, также включаются в данную товарную позицию. Эти продукты используются в фотографии (приготовление тонирующих растворов), в керамике или стекольной промышленности и в медицине.
В данную товарную позицию не включается пурпур кассия, представляющий собой смесь гидроксида олова и коллоидного золота (группа 32); он используется в производстве красок или лаков и, в частности, для окраски фарфора;
(в) прочие соединения. Сульфид золота (Au2S3) – черноватое вещество, которое в сочетании с щелочными сульфидами щелочных металлов образует тиоаураты.
Двойные сульфиты золота и натрия (NaAu(SO3)), а также золота и аммония (NH4Au(SO3)) выпускаются в виде бесцветных растворов и используются при нанесении электролитического покрытия.
Ауротиосульфат натрия используется в медицине.
Цианид золота (AuCN), кристаллический желтый порошок, разлагающийся при нагревании, используется для электролитического золочения и в медицине. Реагирует с цианидами щелочных металлов, давая цианоаураты золота, такие как тетрацианоаурат калия (KAu(CN4)), который представляет собой белую растворимую соль, используемую при нанесении гальванического покрытия.
Ауротиоцианат натрия, кристаллизующийся в виде оранжевых игольчатых кристаллов, используется в медицине и в фотографии (тонирующие растворы).
(3) Соединения рутения. Диоксид рутения (RuO2) – голубой продукт, тетраоксид рутения (RuO4) – оранжевый продукт. Трихлорид рутения (RuCl3) и тетрахлорид рутения (RuCl4) дают двойные хлориды с хлоридами щелочных металлов и аммино– или нитрозокомплексы. Существуют также двойные нитриты рутения или щелочных металлов.
(4) Соединения родия. Гидроксид родия (Rh(OH)3) соответствует оксиду родия (Rh2О3), представляет собой черный порошок. Трихлорид родия (RhCl3) дает хлорородиты с хлоридами щелочных металлов; имеются также сульфат с его комплексными квасцами или фосфатами, нитрат и комплексные нитриты. Также существуют цианородиты и комплексные амминопроизводные или производные щавелевой кислоты.
(5) Соединения палладия. Наиболее стабильный оксид – оксид двухвалентного палладия (PdO), единственный основной оксид. Это черный порошок, разлагающийся при нагревании.
Хлорид двухвалентного палладия (PdCl2), коричневый расплывающийся порошок, растворимый в воде и кристаллизующийся с 2 молекулами воды, используется в производстве керамики, в фотографии и при нанесении гальванического покрытия.
Хлоропалладит калия (K2PdCl4), коричневая соль, хорошо растворимая, используемая как индикатор наличия моноксида углерода, также включается сюда. Существуют также хлоропалладаты, амминосоединения (диаммины палладия), тиопалладаты, палладонитриты, цианопалладиты, палладооксалаты и сульфат двухвалентного палладия.
(6) Соединения осмия. Диоксид осмия (OsO2) – темно–коричневый порошок. Тетраоксид осмия (OsO4) – летучий твердый продукт, кристаллизующийся в виде белых игольчатых кристаллов; он действует на глаза и легкие; используется в гистологии и микрографии. Тетраоксид дает осматы, такие как осмат калия (красные кристаллы), а при обработке аммиаком и гидроксидами щелочных металлов – осмиаматы, такие как осмиамат калия или натрия, представляющие собой желтые кристаллы.
Тетрахлорид осмия (OsCl4) и трихлорид осмия (OsCl3) дают хлороосматы и хлороосмиты щелочных металлов.
(7) Соединения иридия. Кроме оксида иридия, имеются тетрагидроксид иридия (Ir(OH)4) – твердое голубое вещество, хлорид, хлороиридаты и хлороиридиты, двойные сульфаты и амминосоединения.
(8) Соединения платины:
(а) оксиды. Оксид двухвалентной платины (PtO) – фиолетовое или черноватое вещество в виде порошка. Оксид четырехвалентной платины, или диоксид платины (PtO2) образует несколько гидратов, из которых один – тетрагидрат (H2Pt(OH)6) – является комплексной кислотой (гексагидроксоплатиновая кислота), которой соответствуют соли, такие как гексагидроксоплатинаты щелочных металлов. Имеются также соответствующие амминокомплексы;
(б) прочие соединения. Хлорид четырехвалентной платины (PtCl4) существует в виде коричневого порошка или желтого раствора; он используется как реагент. Технический хлорид платины (гексахлороплатиновая кислота) (H2PtCl6) – расплывающиеся призматические кристаллы, окрашенные в коричневато–красный цвет, растворимые в воде; используется в фотографии (тонирующие растворы), при нанесении гальванического покрытия, для глазурования керамики или для получения платиновой губки. Имеются соответствующие амминокомплексы платины.
Также существуют амминокомплексы, соответствующие тетрахлороплатиновой кислоте (H2PtCl4), которая представляет собой красное твердое вещество. Цианоплатиниты калия или бария используются при изготовлении флуоресцирующих экранов для рентгенографии.
(В) АМАЛЬГАМЫ ДРАГОЦЕННЫХ МЕТАЛЛОВ
Это сплавы драгоценных металлов со ртутью. Амальгамы золота или серебра, наиболее известные представители таких продуктов, используются в качестве промежуточных продуктов при получении этих драгоценных металлов.
В данную товарную позицию включаются амальгамы, содержащие как драгоценные металлы, так и недрагоценные металлы (например, некоторые амальгамы, использующиеся в стоматологии); но в данную товарную позицию не включаются амальгамы целиком из недрагоценного металла (товарная позиция 2853).
Соединения ртути определенного или неопределенного химического состава, кроме амальгам, не включаются (товарная позиция 2852).
- +7 (495) 995-95-55
- Telegram-канал
- Вконтакте
- E-mail рассылки
- RSS ленты
Источник: www.alta.ru
Неорганические вещества: примеры и свойства

Ежедневно человек взаимодействует с большим количеством предметов. Они изготовлены из разных материалов, имеют свою структуру и состав. Все, что окружает человека можно разделить на органическое и неорганическое. В статье рассмотрим, что представляют собой такие вещества, приведем примеры. Также определим, какие встречаются неорганические вещества в биологии.
Описание
Неорганическими называются такие вещества, в составе которых нет углерода. Они противоположны органическим. Также к этой группе относят несколько углеродосодержащих соединений, например:
- цианиды;
- оксиды углерода;
- карбонаты;
- карбиды и другие.
Примеры неорганических веществ:
- вода;
- разные кислоты (соляная, азотная, серная);
- соль;
- аммиак;
- углекислый газ;
- металлы и неметаллы.
Неорганическая группа отличается отсутствием углеродного скелета, который характерен для органических веществ. Неорганические вещества по составу принято делить на простые и сложные. Простые вещества составляют немногочисленную группу. Всего их насчитывается примерно 400.

Простые неорганические соединения: металлы
Металлы – простые вещества, соединение атомов которых основывается на металлической связи. Эти элементы имеют характерные металлические свойства: теплопроводность, электропроводность, пластичность, блеск и другие. Всего в этой группе выделяют 96 элементов. К ним относятся:
- щелочные металлы: литий, натрий, калий;
- щелочноземельные металлы: магний, стронций, кальций;
- переходные металлы: медь, серебро, золото;
- легкие металлы: алюминий, олово, свинец;
- полуметаллы: полоний, московий, нихоний;
- лантаноиды и лантан: скандий, иттрий;
- актиноиды и актиний: уран, нептуний, плутоний.
В основном в природе металлы встречаются в виде руды и соединений. Чтобы получить чистый металл без примесей, проводится его очистка. При необходимости возможно проведение легирования или другой обработки. Этим занимается специальная наука – металлургия. Она подразделяется на черную и цветную.

Простые неорганические соединения: неметаллы
Неметаллы – химические элементы, которые не обладают металлическими свойствами. Примеры неорганических веществ:
- вода;
- азот;
- сера;
- кислород и другие.
Неметаллы отличаются большим числом электронов на внешнем энергетическом уровне их атома. Это обуславливает некоторые свойства: повышается способность присоединять дополнительные электроны, проявляется более высокая окислительная активность.
В природе можно встретить неметаллы в свободном состоянии: кислород, хлор, фтор, водород. А также твердые формы: йод, фосфор, кремний, селен.
Некоторые неметаллы имеют отличительное свойство – аллотропию. То есть они могут существовать в различных модификациях и формах. Например:
- газообразный кислород имеет модификации: кислород и озон;
- твердый углерод может существовать в таких формах: алмаз, графит, стеклоуглерод и другие.

Сложные неорганические соединения
Эта группа веществ более многочисленна. Сложные соединения отличаются наличием в составе вещества нескольких химических элементов.
Рассмотрим подробнее сложные неорганические вещества. Примеры и классификация их представлены ниже в статье.
1. Оксиды – соединения, одним их элементов которых является кислород. В группу входят:
- несолеобразующие (например, монооксид углерода, оксид азота);
- солеобразующие оксиды (например, оксид натрия, оксид цинка).
2. Кислоты – вещества, в состав которых входят ионы водорода и кислотные остатки. Например, азотная кислота, серная кислота, сероводород.
3. Гидроксиды – соединения, в составе которых присутствует группа –ОН. Классификация:
- основания – растворимые и нерастворимые щелочи – гидроксид меди, гидроксид натрия;
- кислородосодержащие кислоты – диводород триоксокарбонат, водород триоксонитрат;
- амфотерные – гидроксид хрома, гидроксид меди.
4. Соли – вещества, в составе которых есть ионы металла и кислотные остатки. Классификация:
- средние: хлорид натрия, сульфид железа;
- кислые: гидрокарбонат натрия, гидросульфаты;
- основные: нитрат дигидроксохрома, нитрат гидроксохрома;
- комплексные: тетрагидроксоцинкат натрия, тетрахлороплатинат калия;
- двойные: алюмокалиевые квасцы;
- смешанные: сульфат алюминия калия, хлорид меди калия.
5. Бинарные соединения – вещества, состоящие из двух химических элементов:
- бескислородные кислоты;
- бескислородные соли и другие.

Неорганические соединения, содержащие углерод
Такие вещества традиционно относятся к группе неорганических. Примеры веществ:
- Карбонаты — эфиры и соли угольной кислоты – кальцит, доломит.
- Карбиды – соединения неметаллов и металлов с углеродом – карбид бериллия, карбид кальция.
- Цианиды – соли цианистоводородной кислоты – цианид натрия.
- Оксиды углерода – бинарное соединение углерода и кислорода – угарный и углекислый газы.
- Цианаты – являются производными от циановой кислоты – фульминовая кислота, изоциановая кислота.
- Карбонильные металлы – комплекс металла и монооксида углерода – карбонил никеля.

Свойства неорганических веществ
Все рассмотренные вещества отличаются индивидуальными химическими и физическими свойствами. В общем виде можно выделить отличительные черты каждого класса неорганических веществ:
1. Простые металлы:
- высокая тепло- и электропроводность;
- металлический блеск;
- отсутствие прозрачности;
- прочность и пластичность;
- при комнатной температуре сохраняют твердость и форму (кроме ртути).
2. Простые неметаллы:
- простые неметаллы могут быть в газообразном состоянии: водород, кислород, хлор;
- в жидком состоянии встречается бром;
- твердые неметаллы имеют немолекулярное состояние и могут образовывать кристаллы: алмаз, кремний, графит.
3. Сложные вещества:
- оксиды: вступают в реакцию с водой, кислотами и кислотными оксидами;
- кислоты: вступают в реакцию с водой, основными оксидами и щелочами;
- амфотерные оксиды: могут вступать в реакции с кислотными оксидами и основаниями;
- гидроксиды: растворяются в воде, имеют широкий диапазон температур плавления, могут менять цвет при взаимодействии с щелочами.
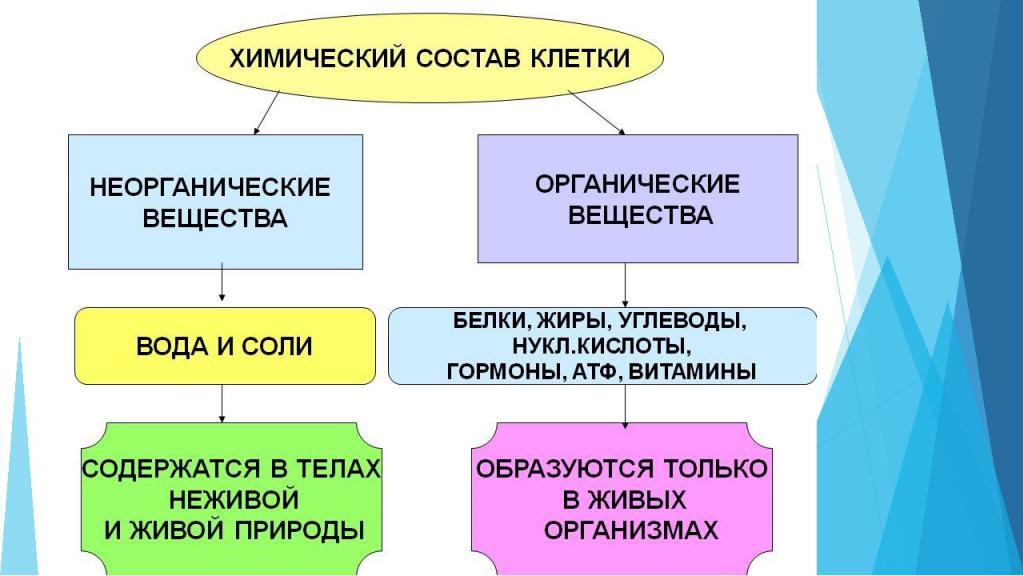
Органические и неорганические вещества клетки
Клетка любого живого организма состоит из множества компонентов. Некоторыми из них являются неорганические соединения:
- Вода. Например, количество воды в клетке составляет от 65 до 95%. Она необходима для осуществления химических реакций, перемещения компонентов, процесса терморегуляции. Также именно вода определяет объем клетки и степень ее упругости.
- Минеральные соли. Могут присутствовать в организме как в растворенном виде, так и в нерастворенном. Важную роль в процессах клетки играют катионы: калий, натрий, кальций, магний — и анионы: хлор, гидрокарбонаты, суперфосфат. Минералы необходимы для поддержания осмотического равновесия, регуляции биохимических и физических процессов, образования нервных импульсов, поддержания уровня свертываемости крови и многих других реакций.
Для поддержания жизнедеятельности важны не только неорганические вещества клетки. Органические компоненты занимают 20-30 % ее объема.
- простые органические вещества: глюкоза, аминокислоты, жирные кислоты;
- сложные органические вещества: белки, нуклеиновые кислоты, липиды, полисахариды.
Органические компоненты необходимы для выполнения защитной, энергетической функции клетки, они служат источником энергии для клеточной активности и запасают питательные вещества, проводят синтез белков, передают наследственную информацию.
В статье были рассмотрены сущность и примеры неорганических веществ, их роль в составе клетки. Можно сказать, что существование живых организмов было бы невозможным без групп органических и неорганических соединений. Они важны в каждой сфере человеческой жизни, а также в существовании каждого организма.
Источник: fb.ru
Сталь это органическое вещество или неорганическое

Ежедневно человек взаимодействует с большим количеством предметов. Они изготовлены из разных материалов, имеют свою структуру и состав. Все, что окружает человека можно разделить на органическое и неорганическое. В статье рассмотрим, что представляют собой такие вещества, приведем примеры. Также определим, какие встречаются неорганические вещества в биологии.
Описание
Неорганическими называются такие вещества, в составе которых нет углерода. Они противоположны органическим. Также к этой группе относят несколько углеродосодержащих соединений, например:
- цианиды;
- оксиды углерода;
- карбонаты;
- карбиды и другие.
Примеры неорганических веществ:
- вода;
- разные кислоты (соляная, азотная, серная);
- соль;
- аммиак;
- углекислый газ;
- металлы и неметаллы.
Неорганическая группа отличается отсутствием углеродного скелета, который характерен для органических веществ. Неорганические вещества по составу принято делить на простые и сложные. Простые вещества составляют немногочисленную группу. Всего их насчитывается примерно 400.

Простые неорганические соединения: металлы
Металлы – простые вещества, соединение атомов которых основывается на металлической связи. Эти элементы имеют характерные металлические свойства: теплопроводность, электропроводность, пластичность, блеск и другие. Всего в этой группе выделяют 96 элементов. К ним относятся:
- щелочные металлы: литий, натрий, калий;
- щелочноземельные металлы: магний, стронций, кальций;
- переходные металлы: медь, серебро, золото;
- легкие металлы: алюминий, олово, свинец;
- полуметаллы: полоний, московий, нихоний;
- лантаноиды и лантан: скандий, иттрий;
- актиноиды и актиний: уран, нептуний, плутоний.
В основном в природе металлы встречаются в виде руды и соединений. Чтобы получить чистый металл без примесей, проводится его очистка. При необходимости возможно проведение легирования или другой обработки. Этим занимается специальная наука – металлургия. Она подразделяется на черную и цветную.

Простые неорганические соединения: неметаллы
Неметаллы – химические элементы, которые не обладают металлическими свойствами. Примеры неорганических веществ:
Неметаллы отличаются большим числом электронов на внешнем энергетическом уровне их атома. Это обуславливает некоторые свойства: повышается способность присоединять дополнительные электроны, проявляется более высокая окислительная активность.
В природе можно встретить неметаллы в свободном состоянии: кислород, хлор, фтор, водород. А также твердые формы: йод, фосфор, кремний, селен.
Некоторые неметаллы имеют отличительное свойство – аллотропию. То есть они могут существовать в различных модификациях и формах. Например:
- газообразный кислород имеет модификации: кислород и озон;
- твердый углерод может существовать в таких формах: алмаз, графит, стеклоуглерод и другие.

Сложные неорганические соединения
Эта группа веществ более многочисленна. Сложные соединения отличаются наличием в составе вещества нескольких химических элементов.
Рассмотрим подробнее сложные неорганические вещества. Примеры и классификация их представлены ниже в статье.
1. Оксиды – соединения, одним их элементов которых является кислород. В группу входят:
- несолеобразующие (например, монооксид углерода, оксид азота);
- солеобразующие оксиды (например, оксид натрия, оксид цинка).
2. Кислоты – вещества, в состав которых входят ионы водорода и кислотные остатки. Например, азотная кислота, серная кислота, сероводород.
3. Гидроксиды – соединения, в составе которых присутствует группа –ОН. Классификация:
- основания – растворимые и нерастворимые щелочи – гидроксид меди, гидроксид натрия;
- кислородосодержащие кислоты – диводород триоксокарбонат, водород триоксонитрат;
- амфотерные – гидроксид хрома, гидроксид меди.
4. Соли – вещества, в составе которых есть ионы металла и кислотные остатки. Классификация:
- средние: хлорид натрия, сульфид железа;
- кислые: гидрокарбонат натрия, гидросульфаты;
- основные: нитрат дигидроксохрома, нитрат гидроксохрома;
- комплексные: тетрагидроксоцинкат натрия, тетрахлороплатинат калия;
- двойные: алюмокалиевые квасцы;
- смешанные: сульфат алюминия калия, хлорид меди калия.
5. Бинарные соединения – вещества, состоящие из двух химических элементов:
- бескислородные кислоты;
- бескислородные соли и другие.

Неорганические соединения, содержащие углерод
Такие вещества традиционно относятся к группе неорганических. Примеры веществ:
- Карбонаты — эфиры и соли угольной кислоты – кальцит, доломит.
- Карбиды – соединения неметаллов и металлов с углеродом – карбид бериллия, карбид кальция.
- Цианиды – соли цианистоводородной кислоты – цианид натрия.
- Оксиды углерода – бинарное соединение углерода и кислорода – угарный и углекислый газы.
- Цианаты – являются производными от циановой кислоты – фульминовая кислота, изоциановая кислота.
- Карбонильные металлы – комплекс металла и монооксида углерода – карбонил никеля.

Свойства неорганических веществ
Все рассмотренные вещества отличаются индивидуальными химическими и физическими свойствами. В общем виде можно выделить отличительные черты каждого класса неорганических веществ:
- высокая тепло- и электропроводность;
- металлический блеск;
- отсутствие прозрачности;
- прочность и пластичность;
- при комнатной температуре сохраняют твердость и форму (кроме ртути).
- простые неметаллы могут быть в газообразном состоянии: водород, кислород, хлор;
- в жидком состоянии встречается бром;
- твердые неметаллы имеют немолекулярное состояние и могут образовывать кристаллы: алмаз, кремний, графит.
- оксиды: вступают в реакцию с водой, кислотами и кислотными оксидами;
- кислоты: вступают в реакцию с водой, основными оксидами и щелочами;
- амфотерные оксиды: могут вступать в реакции с кислотными оксидами и основаниями;
- гидроксиды: растворяются в воде, имеют широкий диапазон температур плавления, могут менять цвет при взаимодействии с щелочами.

Органические и неорганические вещества клетки
Клетка любого живого организма состоит из множества компонентов. Некоторыми из них являются неорганические соединения:
- Вода. Например, количество воды в клетке составляет от 65 до 95%. Она необходима для осуществления химических реакций, перемещения компонентов, процесса терморегуляции. Также именно вода определяет объем клетки и степень ее упругости.
- Минеральные соли. Могут присутствовать в организме как в растворенном виде, так и в нерастворенном. Важную роль в процессах клетки играют катионы: калий, натрий, кальций, магний — и анионы: хлор, гидрокарбонаты, суперфосфат. Минералы необходимы для поддержания осмотического равновесия, регуляции биохимических и физических процессов, образования нервных импульсов, поддержания уровня свертываемости крови и многих других реакций.
Для поддержания жизнедеятельности важны не только неорганические вещества клетки. Органические компоненты занимают 20-30 % ее объема.
- простые органические вещества: глюкоза, аминокислоты, жирные кислоты;
- сложные органические вещества: белки, нуклеиновые кислоты, липиды, полисахариды.
Органические компоненты необходимы для выполнения защитной, энергетической функции клетки, они служат источником энергии для клеточной активности и запасают питательные вещества, проводят синтез белков, передают наследственную информацию.
В статье были рассмотрены сущность и примеры неорганических веществ, их роль в составе клетки. Можно сказать, что существование живых организмов было бы невозможным без групп органических и неорганических соединений. Они важны в каждой сфере человеческой жизни, а также в существовании каждого организма.
Неорганические вещества
Неорганические вещества — это химические вещества, которые не являются органическими, то есть они не содержат углерода (кроме карбидов, цианидов, карбонатов, оксидов углерода и некоторых других соединений, которые традиционно относят к неорганическим).
Классификация
Все вещества делятся на простые (элементарные) и сложные. Простые вещества состоят из одного элемента, а в составе сложных входит не менее двух элементов.
- Простые вещества(элементарные)
- Металлы (
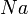 ,
, 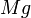 ,
, 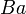 ,
, 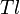 и другие)
и другие) - Переходные металлы (
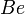 ,
, 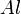 ,
, 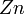 ,
, 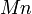 и другие)
и другие) - Неметаллы (
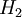 ,
, 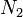 ,
, 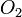 ,
, 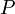 и другие)
и другие)
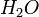 ,
, 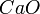 ,
, 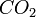 ,
, 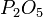 и другие)
и другие)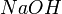 ,
, 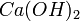 ,
, 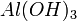 ,
, 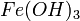 и другие)
и другие)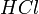 ,
, 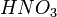 ,
, 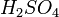 ,
, 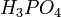 и другие)
и другие)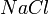 ,
, 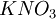 ,
, 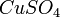 ,
, 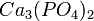 и другие)
и другие)Неорганические вещества разделяют на классы также по составу (двухэлементные, или бинарные, соединения или многокомпонентые соединения), по химическим свойствам (кислотно-основные, окислительно-восстановительные).
Источник: ollimpia.ru