Серебро — мягкий, пластичный и ковкий драгоценный металл снежно-белого цвета. Стандартный электродный потенциал серебра по разным источникам равен 0,799-0,81 В, а его электрохимический эквивалент составляет 4,025 г/(А*ч).
Серебро имеет атомную массу 107,88, плотность 10,49 кг/м 3 и температуру плавления 960,5°С. Теплопроводность серебра в пределах от 0 до 100°С равна 1 кал/(с*см*°С), удельное сопротивление 0,016 Ом*мм. Из всех металлов оно обладает наилучшей тепло- и электропроводимостью.
вердость самородного серебра равна 26 кгс/мм 2 . Микротвердость гальванически осажденных серебряных покрытий возрастает до 590-1370 МПа, а при наличии специальных добавок, вводимых в электролит серебрения, микротвердость возрастает еще в 1,5 — 2 раза.
Насколько серебро химически стойко?
Серебро растворяется в концентрированной азотной кислоте, царской водке, горячей 85% серной кислоте. Серебро неустойчиво в растворах аммиака. Кислород окисляет серебро только при давлении 1,5 МПа и температуре 300° С. Серебро быстро тускнеет в промышленной атмосфере в присутствии одновременно сернистых соединений, кислорода и влаги, покрываясь пленкой сульфидов коричневого и темно-серого цвета. Особенно активно в этом отношении гальванически осажденное серебро. Также серебро может тускнеть в присутствии органических серосодержащих материалов, если длительное время будет находиться вместе с ними в непроветриваемом помещении.
Как покрыть серебром в домашних условиях
Таблица – Характеристики покрытия серебром
Ср1; Ср3; Ср6; Ср9; Ср12; Ср15; Ср18; Ср21; Ср24; Ср27; Ср30 и тд; — стандартное серебрение
Ср3.крц; Ср6.крц; Ср9.крц; Ср12.крц; Ср15.крц; Ср18.крц; Ср21.крц; Ср24.крц; Ср27.крц; Ср30.крц и тд; — серебрение с крацеванием
silver coating — англ. обозначение
3-50мкм (оптимально, возможна и большая толщина)
883-1370 МПа, которая в течение времени может уменьшаться до 558 МПа
Удельное электрическое сопротивление при 18 ° C
Допустимая рабочая температура
Заметное изменение цвета поверхности серебра начинается с толщины сульфидов от 40 нм. При этом максимальная толщина сульфидной пленки составляет 0,3 мкм. Сами по себе пленки сульфида серебра термостойки до 885° С, не растворятся в кислотах и аммиаке, но неустойчивы в 5-10% цианидах.
Химическая активность серебряных покрытий возрастает на шероховатой поверхности.
Серебро устойчиво в соляной кислоте, щелочах, сухом сероводороде. По коррозионной стойкости оно приближается к благородным металлам, не окисляясь на воздухе при обычных условиях.
Во всех соединениях серебро одновалентно, хотя на сегодняшний день этот факт подвергается сомнению — под воздействием озона образуются оксиды двухвалентного серебра. С сероводородом в присутствии влаги и кислорода воздуха серебро образует нерастворимый в воде сульфид серебра. Пленка изменяет свой цвет от радужного через коричневый к черному. Она не разлагается до 885°С и растворяется только в азотной кислоте и аммиаке.
Все соли серебра чувствительны к свету и распадаются под его воздействием с образованием металлического серебра. Поэтому их хранят в непрозрачной таре, установленной в лабораторном шкафу с закрытыми дверцами, а приготовление электролитов ведут в ваннах с крышками или в затемненном помещении.
Вторая жизнь бижутерии. Чистка и Серебрение.

В чем особенности покрытий серебром?
Покрытия серебром являются катодными по отношению ко всем конструкционным материалам и не защищают их поверхность в условиях электрохимической коррозии.
В промышленности серебрение применяется:
- для создания поверхностных слоев высокой электропроводимости;
- для получения антифрикционного покрытия в подшипниках качения и скольжения, в т.ч. в вакууме, инертных средах, маслах;
- для обеспечения хорошей электропроводности в электрических контактах;
- при изготовлении отражателей, т.к. коэффициент отражения белого света для чистого серебра равен 95%;
- для защитно-декоративной отделки бытовых предметов и ювелирных изделий.
К негативным особенностям серебряных покрытий можно отнести:
- склонность к образованию наплывов на покрытии и свариванию контактов;
- плохая переносимость запрессовки в полимеры;
- возможность иглообразования;
- миграция по диэлектрику;
- диффузия на основной металл или на внешний слой покрытия.
Особенно следует рассмотреть вопрос переходного сопротивления электроконтактов с серебряным покрытием. Как упоминалось ранее, на серебряных покрытиях может образовываться сульфидная пленка. Эта пленка обладает ионной и фотоэлектрической проводимостью. Т.е. чем больше она освещена, тем меньшее ее сопротивление.
Такая особенность электропроводимости сульфидов серебра приводит к серьезной нестабильности переходного сопротивления посеребренных электроконтактов в условиях эксплуатации. Если же на контакт приложена малая контактная нагрузка и через него пропускается низкий ток, то проводимость контакта может нарушиться полностью.
На сегодняшний день серебрение из водных растворов производят химически и электрохимически. В связи с тем, что потенциал серебра (+0.8В) намного положительнее потенциала других металлов, невозможно получить прочно сцепленные мелкокристаллические покрытия из растворов простых солей серебра без добавок. На катоде происходит процесс цементации металла с контактным осаждением серебра. Поэтому электролиты на основе простых солей серебра не нашли применения в промышленности.
В свою очередь, распространение получили электролиты на основе комплексных соединений серебра. Комплексообразование позволяет сдвинуть потенциал серебра в отрицательную область, увеличить поляризацию катода, что измельчает кристаллы осадка, увеличить рассеивающую способность. Одновременно с этим комплексообразование снижает предельные плотности тока.
Первым комплексным электролитом был цианистый электролит серебрения. Он отличается наилучшими качествами получаемых покрытий, но является чрезвычайно токсичным. Поэтому одновременно с созданием цианистого электролита начались поиски электролита, не содержащего циан или, хотя бы, не содержащего его в свободном виде.
2. Механизм серебрения из цианистого электролита.
Цианистый электролит серебрения является на сегодняшний день самым изученным и самым лучшим по качеству получаемых из него осадков.
В цианистом растворе в основном образуются комплексы -ди и -три цианаргентаты: [Ag(CN)2] — и [Ag(CN)3] 2 — . В растворе также могут образовываться в незначительном количестве простые гидратированные ионы серебра. Таким образом основными компонентами этого электролита являются цианистый комплекс серебра, цианид щелочного металла и его карбонат, который непосредственно образуется в растворе при реакции цианида с углекислым газом воздуха.
Равновесия в цианидном растворе:
Существует мнение, что при осаждении серебра в прикатодной области образуется коллоидный осадок AgCN по схеме:
Это подтверждается тем, что в покрытии находят цианид серебра.
М. Филгистих и др., измеряя силу тока обмена серебра в зависимости от концентрации свободного цианида пришли к выводу, что при различном содержании свободного цианида разряд ионов серебра будет идти по разным механизмам. При концентрации ионов цианида ниже 6,5 г/л может происходить разряд ионов серебра из AgCN по схеме:
При концентрации цианида выше (13,5 г/л) разряд ионов серебра будет происходить по схеме:
т.е разряд ионов серебра идет непосредственно из комплексного иона. К этому мнению приходят многие исследователи. Об этом же говорят данные потенциометрических измерений, где стационарный потенциал серебра изменяется в зависимости от содержания свободного цианида калия, причем в области низких концентраций изменяется значительно сильнее. Это еще раз подтверждает, что при большом содержании свободного цианида разряд ионов серебра идет непосредственно из комплексного иона.
Рассмотрим поляризационную кривую разряда серебра из цианидной ванны.
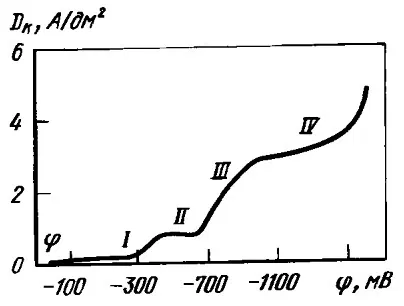
Рисунок 1 — Поляризационная кривая катодного восстановления серебра в цианидном электролите, содержащем: 40 г/л Ag (в пересчете на металл), 15 г/л свободного KCN. Температура 18-22° С
На кривой до предельного диффузионного тока можно выделить три участка, причем катодный осадок на каждом получается разным:
• Участок I. Потенциалы от -0,25 до -0,45 В. При этом емкость двойного электрического слоя имеет мала, осадки гладкие.
• Участок II. Потенциалы от -0,45 до -0,70 В. На кривой имеется перегиб, зернистость осадков повышается.
Участки I и II отвечают элементарному акту разряда, в котором участвуют анионы [Ag(CN)2] — . Перегиб при потенциале -0,45 В обусловлен малой величиной коэффициента переноса и изменением условий разряда ионов при сдвиге потенциалов в сторону более отрицательных значений, при которых возможна десорбция ионов (CN) — с поверхности электрода и ускорение разряда на этих местах ионов [Ag(CN)2] — .
• Участок III. Потенциалы выше -0,70 В. Осадки становятся шероховатыми. Выделяется водород. Могут образовываться анионы [Ag(CN)2]- по химической реакции:
• Участок IV. Преимущественно выделяется водород.
3. Электролиты серебрения.
3.1 Цианистые электролиты матового серебрения.
В таблице 1 и 2 приведены составы электролитов матового цианистого серебрения.
Таблица 1 – Составы электролитов матового серебрения.
(г/л) и режим электролиза
Источник: zctc.ru
Гальваническое покрытие металла серебром

Гальваническое серебрение – популярное направление в сфере гальваники, с помощью которого на детали из металла и сплавов наносится слой серебра необходимой толщины и фактуры. Метод покрытия материала серебром широко применяют по отношению к промышленным изделиям, инструментам и украшениям. Так придают им новые эстетические и функциональные качества.
Гальваническое покрытие серебром: особенности и преимущества
- Выполняется химическое серебрение после тщательной подготовки поверхности, обрабатываемые изделия очищают и обезжиривают, что исключает проблемы появления некачественно обработанных участков или возможного отслаивания покрытия.
- Гальваническое покрытие серебром производится в специальных условиях: после погружения деталей в гальванические ванны, устойчивые к химической среде и агрессивным жидкостям, изделия просушивают. Иногда нанесение серебряного покрытия требует применения специальных барабанов, погружаемых в емкости с целью улучшить производительность.
- Метод гальванического серебрения придает деталям и изделиям особую коррозионную стойкость, улучшает показатели ковкости и электропроводности, повышает их отражательные свойства. Также защитное покрытие серебром обеспечивает металлическим предметам бактерицидные качества, придавая им благородную привлекательность.
Сфера применения гальванического серебрения
- Востребовано гальваническое серебрение не только в области электронной промышленности и при создании радиоприборов.
- Процедуру серебрения применяют для обработки ювелирных украшений, столовых приборов. Поверхность аксессуаров приобретает более аристократичный вид, заметно повышается себестоимость предметов.
- При изготовлении наградных медалей, кубков и сувениров, которые подвергаются прохождению гальванической процедуры, можно сэкономить на затратах по производству этих дизайнерских изделий.
Заказ услуги электро-химического серебрения
Компания «Ленстальинвест» предлагает услуги по гальваническому серебрению в Санкт-Петербурге и регионе. За счет обширных промышленных площадей, наличия высокотехнологичного оборудования в цехах и штата профессионалов нанесение серебряного покрытия на изделия может выполняться по демократичным расценкам.
Солидные наработки, проверенный годами опыт специалистов помогут изменить не только внешний вид деталей и предметов интерьера, но и улучшат гигиенические характеристики изделий. Это повышение ценности украшений, столовых приборов, автоаксессуаров, инструментария и культовой атрибутики, продление их срока эксплуатации.
Наши специалисты применяют гальваническое серебрение фурнитуры и промышленных деталей с целью сделать их стойкими к повреждениям, износу и появлению коррозии. Все заказы предприятие выполняет строго по договору, предлагая выгодные условия сотрудничества и приемлемые цены на услуги.
Источник: lenst.su
Что такое серебрение украшений

Серебро относится к категории благородных металлов, который, помимо своей красоты, определённой ярким блеском, и прочности (высокие показатели химической стойкости), отличается выраженными лечебными свойствами. Именно поэтому серебрение стало таким распространённым процессом. В отличие от любых других составов, серебро может быть нанесено на изделие практически в любом необходимом количестве, даже если понадобится очень большая толщина покрытия.
Серебрение обеспечивает равномерное нанесение материала на основу и гарантирует высокое сцепление. Наиболее часто оно применяется там, где необходима высокая степень отражения. В частности, речь идёт о прожекторах, зеркалах, автомобильных фарах и т.п.

Впрочем, серебрение получило такое распространение не только за счет высоких практических показателей, которыми процесс наделяет изделия, но и благодаря декоративным свойствам. Серебрение позволяет придать изысканный вид украшениям, посуде, а так же прочим металлическим предметам. Главное, чтобы всё было проведено качественно. Это могут гарантировать специалисты нашего научно-технического центра.
Источник: www.technocom-as.ru