Серебро – Ag или Argentum, элемент 11 группы пятого периода таблицы, которую описал Д. И. Менделеев. Это простое вещество – ковкий металл серебристо-серого цвета. Относится к благородным, но на воздухе со временем окисляется, чернеет. Вещество известно с древнейших времен, играет немаловажную роль как промышленное сырье, материал для изысканной бижутерии.
История добычи серебра с древних времен: разное значение и применение
Условный срок знакомства человека с серебром измеряется 6 тысячелетиями. Такой возраст имеют самые древние украшения, обнаруженные при раскопках на Ближнем Востоке. Во времена Вавилона и Ассирии металл считался магическим элементом Луны, имеющим мистическое значение. Эту роль он выполнял также во времена Средневековья: алхимики рассматривали необычного цвета вещество как второй по совершенству металл и неотъемлемую часть Великого Делания.
Ковкость, красота, относительная устойчивость к окислению обеспечили металлу еще одно применение. Для первых на свете денег в виде монет использовался сплав золота или серебра.
Ювелирный мастеркласс. Делаем кольцо из воска. Обработка серебра
Какое-то время металл ценился выше золота, так как последнее слишком пластично, а серебряные украшения служили дольше.
Коэффициент соотношения цены благородных металлов, введенный И. Ньютоном, сыграл в популяризации серебра немаловажную роль.

В 13 веке появилась серебряная посуда и подсвечники, позже – приборы, инструменты. С 19 века, когда человечество освоило электричество, металл, его сплавы стали незаменимыми для изготовления электротехники.
Существует ли 75 проба: что это за металл, серебро или золото, разные гипотезы относительно загадочных цифр в клейме
Открытие химического элемента, его формула и его место в таблице Менделеева. Этимология термина и его перевод
Символ Ag – 47 химический элемент периодической системы Менделеева. Располагается в 5 периоде. Порядковый атомный номер элемента 47, атомарная масса 107, 868, молярный вес – 107,87 г/моль.
Металл существует в виде 2 стабильных изотопов с атомным весом 107 и 109, а также радиоактивного – с весом 110.
Электронная конфигурация необычная: атом серебра состоит из 47 протонов и 47 нейтронов. 47 электронов располагаются на 5 уровнях. Химические свойства зависят от строения последних уровней. Этот элемент является исключением. Расчетная формула предполагает наличие 2 электронов на 1 подуровне 5 уровня и 9 электронов на 3 подуровне 4 уровня. На деле наблюдается проскок: электрон с 5 уровня смещается на 4. Такая трансформация обуславливает основную валентность – 1.
За свою историю серебро в химии получило немало наименований. Однако со средних веков общепринятым стало его произношение на латыни – argentum, что переводится как белый, блистающий.
Форма существования серебра в природе. Главные месторождения
Человечество так рано познакомилось с серебром, поскольку оно часто встречалось как блестящий самородок. Даже в 15 веке все еще находили крупные по размеру залежи: например, серебряная 20 тонная глыба, обнаруженная в 1477 году на территории Шенберга. Но сегодня вещество чаще добывают из пород со сложным составом.
Самые известные месторождения находятся в Мексике, Чили, Китае, Австралии. Фаворитами выступает Перу и Польша – на долю этих стран приходится по 110 тыс. т благородного металла. К первой семерке также относится США.

Запасы вещества на территории России составляют 68 тыс. т, что делает РФ значимым участником серебряного рынка. Известны месторождения Казахстана, Канады, Армении, Индии, Аргентины.
Значение европейского серебра после завоевания Перу и Аргентины уменьшилось. Тем не менее добыча металла продолжается в месторождениях: Германии, Норвегии, Швеции, Австрии. Не снижались темпы разработки руды в Венгрии, Румынии, Чехии.
Минералы природного серебра
Благородный металл. Называют его так не из-за красоты и блеска, а из-за определенной химической инертности. Он медленнее окисляется, дольше сохраняет внешний вид. Однако по сравнению с золотом или платиной, кажется активным, поэтому в земной коре чаще встречается как комплекс серебросодержащих пород.
Известно более 50 минералов металла. В промышленности используются только содержащие достаточно большую долю вещества. Таких набирается не более 20:
- самородки;
- электрум – включает золото и серебро;
- кюстелит – содержит больше белого металла;
- аргентин – соединение с серой;
- прустит – твердый раствор серебра, серы и мышьяка, довольно токсичен;
- бромаргерит – соединение с бромом;
- кераргирит – комплекс хлористых веществ;
- пираргирит и стефанит – включают также серу, сурьму;
- полибазит – дополняется медь;
- фрейбергит – комплекс с медью, серой;
- аргентоярозит – включает железо;
- дискразит – соединение с сурьмой;
- агвиларит – содержит также селен.
На заметку! 70% серебряных месторождений относятся к комплексным.

Физические свойства серебра
Вещество проявляет типичные свойства металла. Он довольно тяжелый, но легче свинца. Очень пластичный. Из него можно выковать тончайшую проволоку или полотно. Кристаллическая решетка гранецентрированная, кубическая, что обуславливает высокую электропроводность.
Техническое серебро: понятие, состав и свойства, где содержится, как получить, стоимость и возможность реализации, вторичное применение и утилизация
| Цвет черты | Серебристо-белый |
| Прозрачность | Непрозрачный |
| Блеск | Металлический |
| Спайность | Нет |
| Твердость (шкала Мооса) | 2,5-3 |
| Прочность | Ковкий, пластичный |
| Плотность | 10,1-11,1 г/куб см |
| Температура плавления | 962 С |
| Излом | Нет |
| Радиоактивность (GRapi) | |
| Магнетизм | Диамагнетик |
Химические характеристики элемента
Химические свойства не слишком разнообразны: вещество достаточно инертно, как благородный металл не растворяется соляной или серной кислотой. Но если создать определенные условия, металл проявит химическую активность.
| O2 | С кислородом воздуха не взаимодействует даже при высоких температурах . Возможно получение оксида при взаимодействии с озоном |
| H2S + O2 | Образует соединение с серой, при наличии даже ее следов |
| Галогены (CL2, I2) | Окисляют до галогенида |
| S | Реакция идет при нагревании до сульфида |
| FeCl3 | Растворяется, образуя хлорид |
| HNO3 | Взаимодействует с горячей концентрированной кислотой |
Вещество склонно к образованию сложных комплексов цианидами, аммиаком, тиосульфатами.

Изучение серебра как химического элемента в школе в рамках предмета Химия
Серебро как химический элемент начинают изучать еще в 8 классе. Он демонстрирует типичные свойства благородного металл, служит своеобразным их образцом.
При изучении неорганической химии с характеристиками вещества знакомятся ближе, разбирают уравнения различных химических реакций. Опыты с материалом показательны и интересны. Однако стоимость реагентов ограничивает количество экспериментов.
Широкое применение химических свойств серебра
Использование вещества чаще основано на его физических свойствах, чем химических, так как его реакционная способность очень ограничена.
- Для контактов электротехнических изделий – драгоценный металл проявляет самую высокую электро- и теплопроводность. Начиная с 19 века его берут для изготовления контактов реле, ламелей, керамических конденсаторов.
- Составляющий различных припоев – благодаря ковкости может буквально соединить собой разные материалы. Металл незаменим при пайке. Составы с большой его долей используются ювелирами, со средней – в технических изделиях, от жидкостных двигателей для ракеты до выключателей. При добавке свинца серебряный припой заменяет собой оловянный.
- Для изготовления электросхем – вещество образует твердые растворы с огромным количеством элементов. Это свойство эксплуатируется при изготовлении, например, катодов гальванических элементов.
- Как драгоценный металл в ювелирной индустрии – отличается роскошной привлекательностью, востребован для ковки самых филигранных, изящных украшений: диадем, серег, колец, браслетов. Чаще используются сплавы с незначительной долей никеля или меди: они более прочны.
- Для чеканки монет, орденов – деньги из серебра чеканили с начала времен. Сегодня материал используют для изготовления юбилейных монет, для чеканки орденов, медалей.
- В фотографии – галогениды вещества на свету разлагаются, обработанная ими поверхность чернеет. Это свойство используется для черно-белой фотографии.
- Для «разгона облаков» перед парадом – опрыскивание небес йодистым серебром вызывает резкое изменение локальной температуры. Таким образом обеспечивают хорошую погоду на ответственных мероприятиях.
- При изготовлении электротехники, электроники покрывают контакты и проводники в высокочастотных цепях, внутреннюю поверхность волноводов. Металл обеспечивает самую высокую электропроводность.
- Для зеркал – амальгама придает зеркалу куда более высокую светоотражающую способность по сравнению с алюминиевой.
- Как катализатор в химических процессах – вещество ускоряет химические реакции промышленного производства, например, при получении эпоксида из этилена.
- Сфера медицины – антибактериальные свойства серебра эксплуатировались во времена Египта и Древней Греции. Металл используется для обеззараживания фильтров кондиционеров, водных очистителей.
Соли, полученные в результате взаимодействия металла с кислотами (нитрат, хлорид), токсичны и применяются в лечебных целях.
Источник: dragomet.com
Серебро химический элемент — основные свойства, месторождения и способы получения металла

Многих людей интересует серебро — химический элемент, который ассоциируется с роскошью, дорогими изделиями, уникальными технологиями в науке и технике. Этот элемент занимает особое место во всей таблице Менделеева, так как всегда, буквально во всей известной человечеству истории, он был материалом для изготовления монет, уникальных предметов быта и прочих ценных вещей.
Серебряные монеты известны еще в самых древних цивилизациях, и они продолжают выпускаться в наше время. Также материал играет важную роль в науке, медицине, промышленности, уникальных технологиях, где выставляются серьезные требования к чистоте используемых веществ. Многих людей интересует не столько химия серебра, как различные связанные с ним поверья, легенды и сказки. Это также занимает большой пласт общечеловеческой культуры и показывает важность рассматриваемого элемента для людей.
История металла
Такое вещество, как серебро, известно человечеству уже очень много тысячелетий, если не сотен тысяч лет. В самых древних мифах, сказаниях и повестях можно встретить упоминания о сделанных из него деньгах и предметах. Свое название материал получил от праславянского наречия, которое было распространено на территории нынешней России, Германии и балтийских стран.

В буквальном переводе оно означает «блестящий», «белый до блеска». Причина такой ранней известности вещества во многих культурах состоит в том, что в отличие от других металлов, которые добывают путем переплавки, руда рассматриваемого материала не требует этой процедуры. Очень часто серебро встречалось древним людям в виде уже готовых к обработке самородков. То есть, не нужны были никакие сложные технологии, чтобы просто брать его и активно использовать в своих целях.
Происхождение названия
Если говорить о названии более подробно, то здесь не все так просто, как было упомянуто выше. Не только в праславянском наречии было слово, похожее на современное «серебро». Открытие специалистов показало, что похожие слова есть в анатолийской группе языков, в языках, распространенных на Ближнем Востоке, а также доиндоевропейских языках стран Европы.
Степень принадлежности слова к той или иной культуре установить очень сложно, если вообще возможно. Существует также и греческое слово, обозначающее серебро árgyros, откуда пошло латинское argentum, принятое международным сообществом в качестве основного названия в международной системе и таблице Менделеева.
Нахождение в природе
Если рассматривать состав земной коры, то в ней на серебра примерно 70 миллиграмм на 1 тонну. Это не так много. С древних времен серебреные монеты и предметы имели высокую ценность, что уже указывает на то, что материал является редким и ценным.

Сплавы материала встречаются реже, нежели чистая руда, но при нынешнем развитии технологий легко обрабатываются с целью выделения необходимой фракции. Интересно отметить, что нередко копателям удавалось обнаружить не руду, а самородки, при этом огромного размера. Истории известен случай, когда был найдет самородок серебра на целых 20 тонн веса! Также находили и другие самородные объекты весом в 500-600 килограммов.
Крупнейшие месторождения серебра в мире
Распределение драгоценного ресурса по поверхности планеты крайне неравномерно. Наиболее интенсивно добыча материала происходит в Перу – это государство является безусловным лидером по количеству получаемого здесь серебра. В среднем, за один год в этой стране добывается около 110 миллионов унций вещества.

Польша является также одним из лидеров по добыче серебра, хотя мало кто догадывается об этом. Здесь добывается около 40,5 миллионов унций серебра.
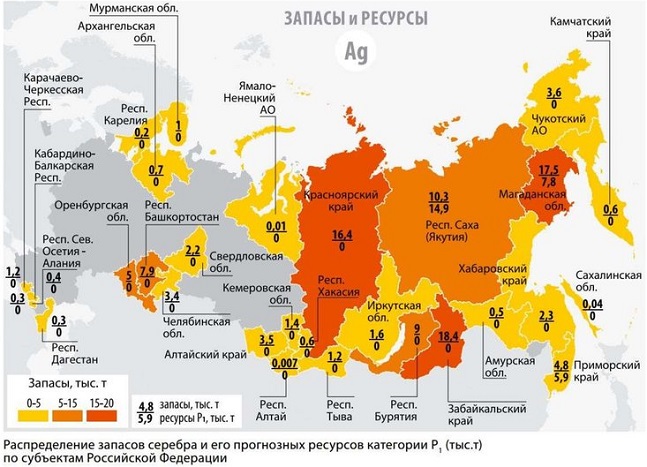
Россия и постсоветские страны имеют около 12-15% от мировых запасов серебра. Горнодобывающая промышленность здесь достаточно развита и дает тонны материала ежегодно. Австралия также входит в перечень счастливчиков, которым повезло с рассматриваемым ресурсом. В остальных частях мира серебра не так много, но всегда есть вероятность обнаружить его пока неизвестные месторождения.
Физические свойства
Масса вещества достаточно высока, что обуславливается тем, что его плотность равна целых 10,5 г/см³. Это больше, чем у другого популярного металла – меди, но меньше, нежели у известного каждому свинца.

Плавление серебра начинается при температуре 962°C, что является достаточно высоким значением. Именно поэтому металл считается тугоплавким и используется, к примеру, для пайки сложных соединений в качестве припоя. В комнатных условиях вещество имеет высокий уровень электропроводности, также отличается высокой теплопроводностью. Оксид, хлорид, сульфид, гидроксид серебра активно используются в научной деятельности и промышленности для решения целого спектра задач.
Химические свойства
Максимальная валентность рассматриваемого металла составляет 1, так как она соответствует номеру группы, где он находится в таблице Менделеева. Ионы серебра слабо реагируют на другие элементы, включая даже серную и соляную кислоту.

Молярная масса равна 107,8 а.е.м. (вес атома такой же), цвет тонкой фольги с чистого материала напоминает фиолетовый, если же берется самородок, то он ярко-светлый, серебристый. Окисление вещества происходит крайне слабо и только в специальных условиях. Для этого приходится использовать плазменные технологии, озон или обработку ультрафиолетовым излучением. Электронная конфигурация серебра выглядит так: 4d^10 5s^1. Кристаллическая решетка – кубическая, а если быть более точным — кубическая гранецентрированная.
Сфера применения серебра
Существует масса применений рассматриваемого материала, благодаря чему он и имеет столь высокую стоимость и авторитет среди самых широких масс людей.

- Техническое применение в науке и промышленности. Надежные контакты для электрического соединения обрабатываются серебром. Так как материал плавится при очень высокой температуре, почти 1000 градусов, то его применяют везде, где важно выдерживать высокотемпературную среду.
- Удельный вес вещества позволяет использовать его в составе различных припоев, к примеру, большой популярностью пользуется медно-серебряный припой.
- Используется среди драгоценных металлов в области создания ювелирных изделий.
- Также металл применяется для создания высококачественных зеркал с повышенной отражающей способностью, в СВЧ-электротехнике.
- Серебро известно своими дезинфицирующими свойствами, поэтому используется для очищения воды от микробов.
В химии существует не одна формула применения серебра для науки, химической промышленности и массы других задач. С его помощью проводятся всевозможные пробы, делаются качественные сварные швы, создается сложная электроника.
Заключение
Argentum – известнейший во всем мире химический элемент, который активно используется в огромном количестве случаев. Значение серебра для современной цивилизации сложно переоценить – во многих сферах деятельности оно буквально незаменимо.
Получение металла из земной породы в наше время поставлено на крупный поток, поэтому человечество получает тонны драгоценного материала для своих нужд ежегодно.
Источник: nauka.club
Серебро

минерал Серебро
Английское название: Silver (silver-3C)
Самородное серебро — очень редкий минерал, который встречается в самых причудливых формах (жгуты, канатики, ветки, трубочки, узоры). Именно поэтому в самородном виде серебро используется в основном в качестве экспонатов для коллекций минералов. Нечасто можно встретить кристаллы самородного серебра.
Они удивительно красивы и имеют обычно кубическую или прямоугольную форму, образуя плотные скопления наподобие друз. При соприкосновении с сероводородом и органическими соединениями самородное серебро темнеет. Зачастую в самородках присутствуют примеси меди, золота, никеля, сурьмы, железа, ртути, которые меняют оттенки кристаллов. Издавна этот минерал использовался людьми для изготовления украшений и предметов быта.
Серебро — это один из драгоценных металлов, который не подвергается воздействию факторов, оказывающих коррозийное и окисляющее влияние. Чистый металл имеет блестящую поверхность белого цвета. Благодаря его блеску, отражающим свойствам и гладкости его использовали до недавних времен в качестве зеркала.
История серебра
Серебро было знакомо людям еще в древности, так как в то время его не приходилось извлекать из руды. Этот металл можно было встретить в природе в самородном виде. Ученые полагают, что первые месторождения серебра находились в Сирии, оттуда его привозили в Египет. Впоследствии серебро стали добывать и в европейских странах, но его запасы быстро иссякли.
После открытия Америки и ее освоения были обнаружены богатейшие месторождения металла в Мексике. А в России первый сереброплавильный завод был построен в Забайкалье в 1701году.
Свойства серебра
Этот благородный металл издревле использовали для изготовления посуды, но материал наделен высокой теплопроводностью, поэтому серебряные столовые изделия нагреваются мгновенно. Дополнительно отличается металл отличной электрической проводимостью и наименьшей температурой плавления среди всех благородных металлов. Несмотря на то, что в чистом виде серебро весьма пластично, оно способно не разрушаться при высоких нагрузках, поэтому его используют при изготовлении ювелирных украшений.
Данный драгоценный металл наделен инертными свойствами, т.е. не взаимодействует с другими составами и веществами. Но из-за высокой реакционной способности оно растворимо во многих кислотах.
Серебро в ювелирной промышленности
Ранее изделия из серебра имели меньшую ценность из-за быстрой потери привлекательности: металл окислялся и темнел, и украшения теряли свой первозданный вид. Сегодня стильный блеск серебряным украшениям придают при помощи белого родия. Благодаря такому покрытию украшения имеют устойчивость к коррозии и механическим повреждениям. Платиновое сияние родия сделало украшения из серебра более благородными, и знаменитые дизайнеры вновь отдают предпочтение этому материалу.
Серебро в промышленности
Серебро обладает уникальными свойствами, поэтому его с успехом применяют на многих производствах. Металл незаменим в электронике, приборостроении, медицине, фотографии и так далее. Ежегодно ученые находят новые способы применения серебра. В современной науке и промышленности используется не только сплав, особое значение имеют его химические соединения.
Физические свойства
Форма кристаллических выделений. Большей частью плотные скопления, характерны также проволочные, волосовидные формы, мелкие чешуйки, листочки, плоские перистые дендриты, зерна неправильной формы.
Кристаллическая структура. Кубическая гранецентрированная решетка.
Класс симметрии. Гексаоктаэдрический — mЗm
Цвет. Серебряно-белый с черной побежалостью. Блеск. Металлический. Прозрачность.
В тонком слое просвечивает. Черта. Серебристо-белая (блестящая). Твердость. 2,5. Плотность. 10-11,1.
Излом. Крючковатый. Сингония. Кубическая. Агрегаты. Большей частью плотные скопления, характерны также проволочные, волосовидные формы, мелкие чешуйки, листочки, плоские перистые дендриты, зерна неправильной формы.
Спайность. Отсутствует, минерал ковкий. П. тр. Плавится. Поведение в кислотах.
Растворяется в азотной кислоте, при добавлении НС1 дает белый осадок хлорида серебра, от сероводорода чернеет.
Свойства минерала
- Удельный вес: 10 — 11,1
- Классы по систематике СССР: Металлы
- Химическая формула: Ag
- Сингония: кубическая
- Цвет: Серебряно-белый с черной побежалостью
- Цвет черты: Серебристо-белая (блестящая)
- Блеск: металлический
- Прозрачность: непрозрачный
- Излом: крючковатый
- Твердость: 2,5
- Ковкость: Да
- Дополнительно: Плавится. Поведение в кислотах. Растворяется в азотной кислоте, при добавлении НС1 дает белый осадок хлорида серебра, от сероводорода чернеет.
Фото минерала



Статьи по теме
- Древние наделяли этот драгоценный металл чудодейственными качествами
Благодаря своим уникальным природным качествам серебро занимает особое место в культурном наследии разных народов. - 75 веков серебра
История использования серебра насчитывает тысячелетия, хотя оно стало известно значительно позднее золота. За это время в мире накопилось множество изделий из серебра - Серебро (англ. Silver, франц. Argent, нем. Silber)
Серебро (англ. Silver, франц. Argent, нем. Silber) стало известно значительно позднее золота, хотя и оно тоже встречается иногда в самородном состоянии. - Самородное серебро
В небольших количествах серебро находили в зоне цементации или иногда — в зоне окисления гидротермальных серебряных жил - Серебро считается самым дешевым драгоценным металлом
Серебро в чистом виде встречается редко. Кроме того, оно быстро окисляется под воздействием влаги, воздуха, поэтому его часто покрывают позолотой, придавая визуальное сходство с золотом
Месторождения минерала Серебро
- Конгсберг
- Дукат месторождение
- Купол месторождение
- Двойное месторождение
- Биркачан
- Россия
- Магаданская область
- Норвегия
- Мангазейское месторождение
- Гана
- Ирак
- Джезказган
- Казахстан
- Соколовско-Сарыбайский ГОК, г. Рудный
Ювелирные камни и металлы
Источник: zegold.ru
